ตัวอย่างปัญหาโมลลิตี: เศษส่วนโมล สูตรและวิธีแก้ปัญหา
ตัวอย่างปัญหาโมลลิตี: เศษส่วนโมล สูตรและวิธีแก้ปัญหา – ในโอกาสนี้ เกี่ยวกับ ความรู้.co.id จะหารือเกี่ยวกับความเลวร้ายด้วยตัวอย่างคำถามต่างๆ และแน่นอนว่าเกี่ยวกับสิ่งอื่นๆ ที่ครอบคลุมประเด็นนี้ด้วย ลองดูการอภิปรายร่วมกันในบทความด้านล่างเพื่อทำความเข้าใจให้ดียิ่งขึ้น
ตัวอย่างปัญหาโมลลิตี: เศษส่วนโมล สูตรและวิธีแก้ปัญหา
โมลลิตีหรือความเข้มข้นโมลเป็นการวัดความเข้มข้นของตัวถูกละลายในสารละลายในแง่ของปริมาณของสารในมวลของตัวทำละลาย สิ่งนี้แตกต่างจากคำจำกัดความของโมลาริตีซึ่งขึ้นอยู่กับปริมาตรของสารละลาย
หน่วยของโมลลิตีทั่วไปในวิชาเคมีคือ โมล/กก. สารละลายที่มีความเข้มข้น 1 โมล/กก. บางครั้งแสดงเป็น 1 โมล คำว่า molality นั้นถูกสร้างขึ้นโดยเทียบเคียงกับ molarity ซึ่งเป็นความเข้มข้นของโมลาร์ของสารละลาย
สามารถทดสอบโมลิลิตีของสารละลายได้โดยการเติมตัวทำละลาย พูดง่ายๆ ก็คือ ค่าโมลลิตี (m) ของสารละลายคือโมลของตัวถูกละลายหารด้วยกิโลกรัมของตัวทำละลาย โมลลิตี้หรือโมลลิตีคือความเข้มข้นของสารละลายซึ่งระบุจำนวนโมล (n) ของตัวถูกละลายในตัวทำละลาย 1 กิโลกรัมหรือ 1,000 กรัม
ความแตกต่างระหว่างโมลาริตีและโมลาริตีคือ ถ้าโมลลิตีเป็นโมลลิตี้หรือความเข้มข้นของโมล (m) แสดงจำนวนโมล ตัวถูกละลายในตัวทำละลาย 1,000 กรัม ส่วนโมลาริตีคือหน่วยบอกจำนวนโมลของตัวถูกละลายในทุก ๆ หนึ่งลิตร สารละลาย. โมลาริตีแสดงด้วยสัญกรณ์ M และหน่วยเป็นโมล/ลิตร
สูตรโมลลิตี้
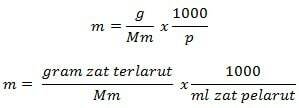
ข้อมูล
m = molality (โมล/กก.)
g = กรัมของตัวถูกละลาย (g)
Mm = มวลโมลาร์ของสาร (g/mol)
P = มวลของตัวทำละลาย (g)
ความสัมพันธ์ทางโมลลิตีกับเปอร์เซ็นต์มวล
เปอร์เซ็นต์มวลเป็นหน่วยของความเข้มข้นที่ใช้กันทั่วไปในสารละลายเคมี ตัวอย่างสารละลายที่เราพบได้ทุกวัน ได้แก่ สารละลายแอลกอฮอล์ 75% และสารละลายกรดอะซิติก 24% เปอร์เซ็นต์มวล คือจำนวนกรัมของตัวถูกละลายในมวลสารละลาย 100 กรัม สมการที่แสดงการคำนวณเปอร์เซ็นต์มวลมีดังนี้

ความสัมพันธ์โมลาริตีกับโมลาริตี
โมลาริตีแสดงจำนวนโมลของตัวถูกละลายในสารละลายหนึ่งลิตร โมลาริตีสามารถแปลงเป็นโมลาริตีได้โดยแปลงปริมาตรของสารละลายเป็นมวลของสารละลาย การแปลงปริมาตรเป็นมวลต้องใช้ข้อมูลความหนาแน่นของสารละลาย (p) ซึ่งสามารถกำหนดได้ดังนี้

เศษส่วนโมล
เศษส่วนโมลคือการวัดความเข้มข้นของสารละลายซึ่งแสดงอัตราส่วนของจำนวนโมลในสารบางชนิดต่อจำนวนโมลทั้งหมดที่มีอยู่ในส่วนประกอบของสารละลาย ส่วนตุ่นแบ่งออกเป็น 2 ส่วน:
เศษส่วนโมลของตัวถูกละลาย (Xt)
สูตรสำหรับเศษส่วนโมลของตัวถูกละลาย (Xt) คือ:

ข้อมูล:
Xt = เศษส่วนโมลของตัวถูกละลาย
Nt = จำนวนโมลของตัวถูกละลาย
Np = จำนวนโมลของตัวทำละลาย
เศษส่วนของตัวทำละลาย (Xp)
สูตรสำหรับส่วนโมลของตัวทำละลาย (Xp) คือ:

ข้อมูล
Xp = ส่วนโมลของตัวทำละลาย
Nt = จำนวนโมลของตัวถูกละลาย
Np = จำนวนโมลของตัวทำละลาย
ผลรวมของเศษส่วนโมลของตัวถูกละลายและตัวทำละลายคือ 1
Xt + Xp = 1
ตัวอย่างของปัญหา Molality และวิธีแก้ไข
ปัญหา 1
สารละลายที่มี NaOH 4 กรัม (Ar Na = 23 กรัม/โมล, Ar O = 16 กรัม/โมล และ Ar H = 1 กรัม/โมล) ละลายในน้ำ 250 กรัมมีค่าเป็นเท่าใด
เสร็จสิ้น:
เป็นที่รู้จัก:
มวลของ NaOH = 4 กรัม
ArNa = 23 กรัม/โมล
ArO = 16 ก./โมล
ArH = 1 กรัม/โมล
มวลน้ำ = 250 กรัม = 0.25 กก
ถาม: m = ?
คำตอบ:
นาย. NaOH = 40 กรัม/โมล
จำนวนโมลของ NaOH = มวล/นาย
จำนวนโมลของ NaOH = 4 gr/(40 gr/mol)
จำนวนโมลของ NaOH = 0.1 โมล
m = จำนวนโมล/p
m = 0.1 โมล / 0.25 กก
ม. = 0.4 ม
ปัญหาที่ 2
สารละลาย HCl 37% (w/w) มีความเข้มข้นเท่าใด (Ar H = 1 ก./โมล, Ar Cl = 35.5 ก./โมล)
เสร็จสิ้น:
เป็นที่รู้จัก:
มวลของ HCl = 37%
ArH = 1 กรัม/โมล
ArCl = 35.5 ก./โมล
ถาม: m = ?
คำตอบ:
นาย. HCl = 36.5 กรัม/โมล
สมมติว่ามวลของสารละลายคือ 100 กรัม ดังนั้นมวลของ HCl คือ:
มวล HCl = 37% x 100 กรัม
มวลของ HCl = 37 กรัม
มวลของตัวทำละลาย = มวลของสารละลาย – มวลของ HCl
มวลของตัวทำละลาย = 100 กรัม – 37 กรัม
มวลของตัวทำละลาย = 63 กรัม = 0.063 กก
จำนวนโมลของ HCl = มวล/นาย
จำนวนโมลของ HCl = 37 กรัม /(36.5 กรัม/โมล)
จำนวนโมลของ HCl = 1.01 โมล
m = จำนวนโมล/มวลของตัวทำละลาย
m = 1.01 โมล /0.063 กก
ม. = 16.03 ม
ปัญหา 3
หาค่าโมลิตีของสารละลายที่เตรียมโดยการละลายยูเรีย CO(NH2)2 12 กรัมในน้ำ 250 กรัม
เสร็จสิ้น:
เป็นที่รู้จัก:
มวลของยูเรีย = 12 กรัม
มิสเตอร์ยูเรีย = 60 ก./โมล
มวลของตัวทำละลาย = 250 กรัม = 0.25 กก
ถาม: m = ?
โฆษณา
คำตอบ:
จำนวนโมลของยูเรีย = มวล/นาย
จำนวนโมลของยูเรีย = 12 กรัม /(60 กรัม/โมล)
จำนวนโมลของยูเรีย = 0.2 โมล
m = จำนวนโมล/มวลของตัวทำละลาย
m = 0.2 โมล / 0.25 กก
ม. = 0.8 ม
ปัญหาที่ 4
สารละลายแอลกอฮอล์ที่มีเอทานอล 23 % โดยมวลมีค่าเท่าใด (Mr = 46)
คำตอบ:
เป็นที่รู้จัก:
มวลเอทานอล = 23%
Mr เอทานอล = 46 ก./โมล
ถาม: m = ?
เสร็จสิ้น:
ตัวอย่างเช่น มวลของสารละลายแอลกอฮอล์คือ 100 กรัม มวลของเอทานอลคือ:
มวลเอทานอล = 23% x 100 กรัม
มวลเอทานอล = 23 กรัม
มวลของตัวทำละลาย = มวลของสารละลาย – มวลของเอทานอล
มวลของตัวทำละลาย = 100 กรัม – 23 กรัม
มวลของตัวทำละลาย = 77 กรัม = 0.077 กก
จำนวนโมลของเอทานอล = มวล/นาย
จำนวนโมลของเอทานอล = 23 กรัม /(46 กรัม/โมล)
จำนวนโมลของเอทานอล = 0.5 โมล
m = จำนวนโมล/มวลของตัวทำละลาย
m = 0.5 โมล /0.077 กก
ม. = 6.49 ม
ปัญหา 5
คำนวณความเข้มข้น (% โดยมวล) ของกลูโคสในสารละลายกลูโคส 2 โมล
เสร็จสิ้น:
เป็นที่รู้จัก:
m = 2 โมล = 2 โมล/กก. = 0.002 โมล/กรัม
มิสเตอร์กลูโคส = 180 กรัม/โมล
ถาม: มวลของกลูโคส (%) = ?
คำตอบ:
โมลของกลูโคส = มวล/นาย
โมลของกลูโคส = มวลของกลูโคส/(180 ก./โมล)
โมลของกลูโคส = มวลของกลูโคส x 0.005 โมล/กรัม
แทนค่าโมลของกลูโคสในสมการต่อไปนี้
m = โมลของกลูโคส/มวลของตัวทำละลาย
0.002= มวลของกลูโคส x 0.005/มวลของตัวทำละลาย
o, oo2/o, oo5 = มวลของกลูโคส/มวลของตัวทำละลาย
2/5 = มวลของกลูโคส/มวลของตัวทำละลาย
ดังนั้น อัตราส่วนโดยมวลของกลูโคส: มวลของตัวทำละลาย = 2:5 ในขณะที่อัตราส่วนโดยมวลของกลูโคส: มวลของสารละลาย = 2:7
ดังนั้น,
% มวลของกลูโคส = (มวลของกลูโคส/มวลของสารละลาย) x100%
% โดยมวลของกลูโคส = (2/7) x 100%
% มวลกลูโคส = 28.57 %
ปัญหา 6
สารละลายที่มี NaOH 8 กรัม (Ar Na = 23 กรัม/โมล, Ar O = 16 กรัม/โมล และ Ar H = 1 กรัม/โมล) ละลายในน้ำ 250 กรัมมีค่าเป็นเท่าใด
การอภิปราย
เป็นที่รู้จัก:
มวลของ NaOH = 8 กรัม
ArNa = 23 กรัม/โมล
ArO = 16 ก./โมล
ArH = 1 กรัม/โมล
มวลน้ำ = 250 กรัม = 0.25 กก
ต้องการ: Molality (m)….?
คำตอบ:
นาย. NaOH = 40 กรัม/โมล
จำนวนโมลของ NaOH = มวล/นาย
จำนวนโมลของ NaOH = 8 gr/(40 gr/mol)
จำนวนโมลของ NaOH = 0.2 โมล
m = จำนวนโมล/p
m = 0.2 โมล / 0.25 กก
ม. = 0.8 ม
ปัญหา 6
หาค่าโมลิตีของสารละลายที่เตรียมโดยการละลายยูเรีย CO(NH2)2 15 กรัมในน้ำ 250 กรัม
การอภิปราย
เป็นที่รู้จัก:
มวลของยูเรีย = 15 กรัม
มิสเตอร์ยูเรีย = 60 ก./โมล
มวลตัวทำละลาย = 250 กรัม = 0.25 กก
ต้องการ: Molality (m)…. ?
คำตอบ:
จำนวนโมลของยูเรีย = มวล/นาย
โมลทั้งหมดของยูเรีย = 15 กรัม / 60 กรัม/โมล
จำนวนโมลของยูเรีย = 0.25 โมล
m = จำนวนโมล/มวลของตัวทำละลาย
m = 0.25 โมล / 0.25 กก
ม = 1 ม
ปัญหา 7
สารละลาย HCl 37% (w/w) มีความเข้มข้นเท่าใด (Ar H = 1 ก./โมล, Ar Cl = 35.5 ก./โมล)
การอภิปราย
เป็นที่รู้จัก:
มวลของ HCl = 37%
ArH = 1 กรัม/โมล
ArCl = 35.5 ก./โมล
ต้องการ: Molality (m)…?
คำตอบ:
นาย. HCl = 36.5 กรัม/โมล
สมมติว่ามวลของสารละลายคือ 100 กรัม ดังนั้นมวลของ HCl คือ:
มวล HCl = 37% x 100 กรัม
มวลของ HCl = 37 กรัม
มวลของตัวทำละลาย = มวลของสารละลาย – มวลของ HCl
มวลของตัวทำละลาย = 100 กรัม – 37 กรัม
มวลของตัวทำละลาย = 63 กรัม = 0.063 กก
จำนวนโมลของ HCl = มวล/นาย
จำนวนโมลของ HCl = 37 กรัม /(36.5 กรัม/โมล)
จำนวนโมลของ HCl = 1.01 โมล
m = จำนวนโมล/มวลของตัวทำละลาย
m = 1.01 โมล /0.063 กก
ม. = 16.03 ม

ปัญหา 8
หาปริมาณ (กรัม) ของ NaOH ที่ต้องละลายในน้ำ 1 ลิตร (น้ำ = 1.00 g/mL) เพื่อให้ได้ NaOH 0.25 m
การอภิปราย
เป็นที่รู้จัก:
น้ำ 1 ลิตร = 1,000 มล. = 1,000 กรัม (เนื่องจาก ρ ของน้ำ = 1.00 กรัม/มล.)
mNaOH = 0.25 ม
นายนะโอ = 40
ถาม: แกร…?
คำตอบ:
mNaOH = gr / Mr x 1,000 / P
0.25 = กรัม/40 x 1,000/1,000
0.25 = ก./40
กรัม = 0.25 x 40
กรัม = 10 กรัม
ดังนั้นปริมาณ NaOH ที่ต้องการคือ 10 กรัม
ปัญหา 9
กำหนดว่าต้องใช้น้ำกี่มล. เพื่อละลาย H2SO4 4.9 กรัม ซึ่งมีความเข้มข้น 0.25 M (Ar H = 1; ส = 32; ต =16)!
การอภิปราย
เป็นที่รู้จัก:
mH2SO4 = 0.25
นาย H2SO4 = 98
กรัม = 4.9 กรัม
ถาม: พี???
คำตอบ:
m = gr/Mr x 1,000/P
0.25 = 4.9/98 x 1,000/หน้า
p = 20 กรัม (20 มล.)
ดังนั้นปริมาตรของน้ำคือ 20 มล.
ปัญหา 10
ต้องใช้น้ำปริมาณเท่าใดในการเตรียมสารละลาย 1.2 ม. โดยใช้ NaCl 0.6 โมล
การอภิปราย
molality (ม.) = 1.2 มม. =
นพี
1,2 =
0,6พี
พี=
0,61,2
= 0.5 กก
ดังนั้น มวลของน้ำ (มวลของตัวทำละลาย) ที่ต้องการคือ 0.5 กก
ปัญหา 11
สมมติว่ามีตัวถูกละลาย 2 โมลในตัวทำละลาย 1 ลิตร จะมีโมลลิตีเท่าใด
การอภิปราย
โมลที่ละลาย (n) = 2 โมล =
นพี
เมตร =
21
= 2 ม
คำนวณค่าโมลิตีของ KBr 25 กรัม (Mr = 119) ที่ละลายในน้ำบริสุทธิ์ 750 มล.
การอภิปราย
ตัวถูกละลาย = 25 กรัม
นาย = 119
ตัวทำละลาย (P) = 750 mL = 750 กรัม (เพราะ ρ ของน้ำ = 1.00 g/mL) = 0.75 kgn =
สารที่ละลายนาย
n =
25119
= 0.21 โมล
เมตร =
นพี
เมตร =
0,210,75
= 0.28 ม
ดังนั้นการทบทวนจาก เกี่ยวกับ ความรู้.co.id เกี่ยวกับ ตัวอย่างของปัญหา Molality , หวังว่าจะสามารถเพิ่มความเข้าใจและความรู้ของคุณ ขอบคุณที่เข้ามาเยี่ยมชมและอย่าลืมอ่านบทความอื่นๆ
รายการเนื้อหา
คำแนะนำ:
- เซลลูโลสคือ: ความหมาย ประเภท โครงสร้าง คุณสมบัติ และ... เซลลูโลสคือ: ความหมาย ประเภท โครงสร้าง คุณสมบัติและหน้าที่ - เซลลูโลสเป็นสารประกอบคล้ายเส้นใย และพบในผนังเซลล์ป้องกันของพืช เพื่อให้เข้าใจดีขึ้น แน่นอน เราจะหารือ...
- √ ความหมายของการขยายความยาว สูตร พื้นที่ และปริมาตรของสาร... คำจำกัดความของการขยายตัวแบบยาว สูตร พื้นที่ และปริมาตรของของแข็ง - ในการสนทนานี้ เราจะอธิบายเกี่ยวกับการขยายตัวแบบยาว ซึ่งรวมถึงแนวคิดเรื่องการขยายตัวตามยาว สูตรการขยายตัวตามยาว พื้นที่ ปริมาตรของสสาร...
- หน่วยวัด: ความหมาย, การแปลงหน่วยความยาว, วิธี... บันไดวัด: ความหมาย การแปลงหน่วยความยาว วิธีใช้ และตัวอย่างคำถาม - มีอะไรบ้าง บันไดขนาด หมายความว่าอย่างไรและใช้งานอย่างไร ครั้งนี้ทาง Knowledge.co.id จะ หารือเกี่ยวกับมัน ...
- พันธะโควาเลนต์: ความหมาย ลักษณะ ประเภท สูตร... พันธะโควาเลนต์: ความหมาย ลักษณะ ประเภท สูตรทางเคมี และคุณสมบัติของสารประกอบ - พันธะโควาเลนต์คืออะไร? ในโอกาสนี้ Seputarknowledge.co.id จะหารือเกี่ยวกับเรื่องนี้และแน่นอนว่าเกี่ยวกับสิ่งอื่นๆ ด้วย ครอบคลุมมัน อนุญาต…
- สุนทรพจน์ด้านสิ่งแวดล้อม: ความหมาย วัตถุประสงค์ ลักษณะ และ... สุนทรพจน์ด้านสิ่งแวดล้อม: ความหมาย วัตถุประสงค์ ลักษณะ และตัวอย่าง - ข้อความของสุนทรพจน์ด้านสิ่งแวดล้อมมีโครงสร้างอย่างไร อะไรดีและถูกต้อง ในโอกาสนี้ Seputarknowledge.co.id จะมาพูดคุย และแน่นอนว่าเรื่องต่างๆ ที่…
- สูตรกรวย ลักษณะ คุณสมบัติ องค์ประกอบ และตัวอย่างปัญหา สูตรทรงกรวย ลักษณะ คุณสมบัติ องค์ประกอบ และตัวอย่าง ปัญหา - วิธีคำนวณพื้นที่และปริมาตรของรูปทรง cone space? ในโอกาสนี้ Seputarknowledge.co.id จะหารือเกี่ยวกับเรื่องนี้และแน่นอนเกี่ยวกับสิ่งอื่นๆ ที่…
- สูตรความหนืด: คำจำกัดความของความหนืด ค่าสัมประสิทธิ์ และ... สูตรความหนืด: นิยามความหนืด ค่าสัมประสิทธิ์ และปัจจัยที่มีอิทธิพล - สูตรความหนืดเป็นอย่างไร ใช่หรือไม่ ความหนืดคือการวัดค่าความต้านทานของของไหลที่เปลี่ยนแปลงโดยความเค้นหรือโดย ความดัน. ในโอกาสนี้ Seputarknowledge.co.id…
- หน่วยน้ำหนัก: ความหมาย บันไดการแปลง และตัวอย่าง... หน่วยน้ำหนัก: ความหมาย บันไดการแปลง และตัวอย่างปัญหา - หน่วยน้ำหนักคืออะไร ในโอกาสนี้ เกี่ยวกับ knowledge.co.id จะพูดคุยถึงเรื่องนี้ รวมถึงความเข้าใจและแน่นอนเรื่องอื่นๆ ด้วย ครอบคลุมมัน อนุญาต…
- โมเมนต์ความเฉื่อย: ความหมาย ปัจจัย สมการของรูปแบบ... โมเมนต์ความเฉื่อย: ความหมาย ปัจจัย สมการในรูปของวัตถุและตัวอย่างปัญหา - ความหมาย กับโมเมนต์ความเฉื่อย ในโอกาสนี้ Se เกี่ยวกับ knowledge.co.id จะกล่าวถึง และแน่นอนเกี่ยวกับ วัตถุ…
- การเคลื่อนที่แบบวงกลมที่เปลี่ยนแปลงสม่ำเสมอ: ความหมาย ขนาด... การเคลื่อนที่แบบวงกลมที่เปลี่ยนแปลงอย่างสม่ำเสมอ: ความหมาย ปริมาณทางกายภาพ สูตร และตัวอย่างปัญหา - การเคลื่อนที่คืออะไร การเปลี่ยนแปลงแบบวงกลมเป็นประจำและตัวอย่าง ในโอกาสนี้ Seputarknowledge.co.id แน่นอนเกี่ยวกับ...
- อินทิกรัลไม่จำกัด: ความหมาย สูตร คุณสมบัติ และตัวอย่าง... อินทิกรัลไม่จำกัด: ความหมาย สูตร คุณสมบัติ และตัวอย่างปัญหา - อินทิกรัลไม่ จำกัด หมายความว่าอย่างไร แน่นอนและวิธีการคำนวณการดำเนินการทางคณิตศาสตร์? จะ…
- ความหมายของวิธีการเรียนรู้ ลักษณะ จุดประสงค์ ประเภท และ... ความหมายของวิธีการเรียนรู้: ลักษณะเฉพาะ วัตถุประสงค์ ประเภท และการอภิปราย - วิธีการหมายถึงอะไร การเรียนรู้ ในโอกาสนี้ Seputarknowledge.co.id จะหารือเกี่ยวกับเรื่องนี้และแน่นอนเกี่ยวกับสิ่งอื่นๆ อีกด้วย…
- สมดุลเคมี: ความหมาย กฎ สูตร ปัญหาตัวอย่าง สมดุลเคมี: นิยาม กฎ สูตร ปัญหาตัวอย่าง - เราจะอธิบายในการสนทนานี้ เกี่ยวกับสมดุลเคมี กฎของสูตร พร้อมตัวอย่างสมดุลเคมีอย่างครบถ้วน และ...
- สารละลายกรด-เบส: ความหมาย ทฤษฎีกรด-เบส คุณสมบัติ และ... สารละลายกรด-เบส: คำนิยาม ทฤษฎีกรด-เบส คุณสมบัติและประเภท - สารละลายกรดและเบสเป็นสารประกอบเคมีสองกลุ่มที่พบและใช้กันอย่างแพร่หลายในชีวิตประจำวัน
- Build Space – คำจำกัดความ สูตร และหลากหลาย... พื้นที่สร้าง – ความหมาย สูตร และประเภทต่างๆ ในโอกาสนี้ ขอทบทวนสาระทางคณิตศาสตร์เกี่ยวกับรูปทรงเรขาคณิตทั้งจากความเข้าใจและอื่นๆ เดี๋ยวค่อยว่ากัน...
- √ ตัวบ่งชี้ความเป็นกรด-เบส: ความหมาย ประเภท และตัวอย่าง ตัวบ่งชี้ความเป็นกรด-เบส: ความหมาย ประเภท และตัวอย่าง - ในโอกาสนี้ Around Knowledge จะกล่าวถึงตัวบ่งชี้ความเป็นกรด-เบส ซึ่งในการอภิปรายนี้จะอธิบายถึงความหมายของตัวบ่งชี้กรด...
- กฎของบอยล์: ความหมาย สูตร การนำไปใช้ และตัวอย่าง... กฎของบอยล์: ความหมาย สูตร การนำไปใช้ และตัวอย่างปัญหา - ในการสนทนานี้ เราจะอธิบายเกี่ยวกับกฎของบอยล์ ซึ่งรวมถึงความหมายของกฎของบอยล์ สูตรกฎของบอยล์ การประยุกต์ใช้...
- เรื่องสั้นที่สร้างแรงบันดาลใจ: ความหมาย เคล็ดลับในการเขียน และตัวอย่าง เรื่องสั้นสร้างแรงบันดาลใจ: ความหมาย เคล็ดลับในการเขียน และตัวอย่าง - เรื่องสั้นสร้างแรงบันดาลใจคืออะไร บน ในโอกาสนี้ Seputarknowledge.co.id จะกล่าวถึงเรื่องสั้นแห่งมิตรภาพและเรื่องอื่นๆ หรือไม่ เกี่ยวกับมัน. มาดูกัน…
- ความหมายของความดัน: ประเภทของความดัน สูตร และตัวอย่างปัญหา ความหมายของความดัน: ประเภทของความดัน สูตร และปัญหาตัวอย่าง - ความดันคืออะไร ที่ ในโอกาสนี้ รอบ Knowledge.co.id เราจะมาคุยกันว่าแรงกดดันคืออะไรและองค์ประกอบอื่นๆ คืออะไร ครอบคลุมมัน มาดูกัน…
- ของไหลไดนามิก: ประเภท คุณลักษณะ สมการเบอร์นูลลี ทฤษฎีบท... ของไหลไดนามิก: ประเภท คุณสมบัติ สมการของแบร์นูลลี ทฤษฎีบทของทอริเชลลี สูตรและตัวอย่างปัญหา - คืออะไร ของไหลไดนามิกและประเภทของมัน? เกี่ยวกับ…
- ความหนาแน่นของน้ำ: ความหมาย สูตร และตัวอย่าง ความหนาแน่นของน้ำ: ความหมาย สูตร และตัวอย่าง - ความหนาแน่นของน้ำคืออะไร? มาดูกันเลย…
- ความหมายของปริมาณ หน่วย การวัด และตัวอย่าง... คำจำกัดความของปริมาณ หน่วย การวัด และตัวอย่าง (สมบูรณ์) - ในแนวคิดฟิสิกส์พื้นฐาน แน่นอนว่าเราได้รู้จักกับบางสิ่งที่เกี่ยวข้องกับชีวิตประจำวัน เช่น วัดส่วนสูง ชั่งมวล วัดความกว้าง...
- ตัวอย่างงานวิทยาศาสตร์: หน้าที่และกฎของภาษา ตัวอย่างเอกสารทางวิทยาศาสตร์: หน้าที่และกฎของภาษา - ตัวอย่างการเขียนเอกสารทางวิทยาศาสตร์ในรูปแบบที่ดีและถูกต้องคืออะไร ก่อนหน้านี้ Seputar the knowledge.co.id ได้กล่าวถึงงานทางวิทยาศาสตร์: ความหมาย ลักษณะเฉพาะ ประโยชน์…
- ตัวอย่างของรูปทรงแบน ประเภท ลักษณะ และสูตรของรูปทรงแบน ตัวอย่างของ Flat Shapes: ประเภท คุณสมบัติ และสูตรของ Flat Shapes - ตัวอย่างของ Flat Shapes คืออะไร?
- ตัวอย่างคำถามพลศึกษาสำหรับคลาส 11 (XI) SMA/MA/SMK ภาคเรียนที่ 1 และ 2 ตัวอย่างคำถามพลศึกษาสำหรับคลาส 11 (XI) สำหรับ SMA/MA/SMK ภาคการศึกษาที่ 1 และ 2 (2019 และ 2020) - ในโอกาสนี้ Seputarknowledge.co.id จะหารือตัวอย่างคำถามพลศึกษาสำหรับคลาส 11 แบบปรนัยและเรียงความ …
- ปริมาณน้ำฝนคือ: 12 คำจำกัดความตามผู้เชี่ยวชาญ ประเภท... ปริมาณน้ำฝนคือ: 12 คำจำกัดความตามประเภทผู้เชี่ยวชาญและปัจจัย - ในการสนทนานี้ ความรู้รอบตัวจะอธิบายเกี่ยวกับปริมาณน้ำฝน ฝนเป็นเหตุการณ์ทางภูมิอากาศที่เกิดขึ้นตามธรรมชาติ...
- √ ความหมายของสารประกอบทางเคมี ลักษณะ ประเภท และระบบการตั้งชื่อ... คำจำกัดความของสารเคมี ลักษณะ ประเภท ระบบการตั้งชื่อที่สมบูรณ์ - ในการสนทนานี้ เราจะอธิบายเกี่ยวกับสารประกอบทางเคมี ครอบคลุมความหมาย ลักษณะ ชนิด และศัพท์เฉพาะของสารเคมี พร้อมอภิปราย...
- สารเดี่ยวคือ: ความหมาย องค์ประกอบ และสารประกอบ สารเดี่ยวคือ: คำจำกัดความ องค์ประกอบ และสารประกอบ - สารเดี่ยวหมายถึงอะไร? มาดูการอภิปรายร่วมกัน...
- ระนาบเอียง: ความหมาย สูตร ความได้เปรียบเชิงกล และ... ระนาบเฉียง: ความหมาย สูตร ข้อดีเชิงกล และตัวอย่างปัญหา - ระนาบหมายถึงอะไร เอียงและวิธีคำนวณทางฟิสิกส์? โดยธรรมชาติ…
- การแปลงหน่วย: ความหมาย, ปัจจัย, ความยาว, มวล, เวลา,... การแปลงหน่วย: ความหมาย ปัจจัย ความยาว มวล เวลา ปริมาตร และความดัน - การแปลงหน่วยคืออะไร, ในโอกาสนี้ Seputarknowledge.co.id จะหารือเกี่ยวกับเรื่องนี้ รวมถึงปัจจัย ประเภท และแน่นอนสิ่งอื่นๆ ที่…
