Primer problema molalnosti: molski delež, formula in rešitev
Primer problema molalnosti: molski delež, formula in rešitev – Ob tej priložnosti O znanju.co.id bo razpravljal o molalnosti z več primeri vprašanj in seveda o drugih stvareh, ki to prav tako pokrivajo. Oglejmo si skupaj razpravo v spodnjem članku, da jo bomo bolje razumeli.
Primer problema molalnosti: molski delež, formula in rešitev
Molnost ali molalna koncentracija je merilo koncentracije topljenca v raztopini glede na količino snovi v določeni masi topila. To se razlikuje od definicije molarnosti, ki temelji na določenem volumnu raztopine.
Skupna enota molalnosti v kemiji je mol/kg. Raztopina s koncentracijo 1 mol/kg je včasih izražena tudi kot 1 mol. Izraz molalnost je oblikovan po analogiji z molarnostjo, ki je molska koncentracija raztopine.
Molnost raztopine je mogoče preizkusiti z dodajanjem nekaj topila. Preprosteje, molalnost (m) raztopine je število molov topljenca, deljeno s kilogrami topila. Molnost ali molalnost je koncentracija raztopine, ki pove število molov (n) topljene snovi v 1 kg ali 1000 gramih topila.
Razlika med molalnostjo in molarnostjo je v tem, da če je molalnost molalnost ali molalna koncentracija (m), izraža število molov topljenec v 1000 gramih topila, medtem ko je molarnost izjava o številu molov topljenca v vsakem litru rešitev. Molarnost je predstavljena z oznako M, enote pa so mol/liter.
Formula molalnosti
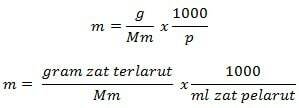
Informacije
m = molalnost (mol/kg)
g = grami topljenca (g)
Mm = molska masa snovi (g/mol)
P = masa topila (g)
Razmerje molalnosti z masnim odstotkom
Masni odstotek je enota koncentracije, ki se običajno uporablja v kemičnih raztopinah. Primera raztopin, ki jih lahko najdemo vsak dan, sta 75% raztopina alkohola in 24% raztopina ocetne kisline. Masni odstotek je število gramov topljenca v 100 gramih mase raztopine. Enačba, ki prikazuje izračun masnega odstotka, je naslednja:

Razmerje med molarnostjo in molarnostjo
Molarnost izraža število molov topljenca v enem litru raztopine. Molarnost lahko pretvorimo v molalnost s pretvorbo volumna raztopine v maso raztopine. Za pretvorbo prostornine v maso so potrebni podatki o gostoti raztopine (p), ki jih je mogoče formulirati na naslednji način:

Molska frakcija
Molski delež je merilo koncentracije raztopine, ki izraža razmerje med številom molov v nekaterih snoveh in skupnim številom molov, prisotnih v komponentah raztopine. Molska frakcija je razdeljena na 2 dela:
Molski delež topljenca (Xt)
Formula za molski delež topljenca (Xt), in sicer:

Informacije:
Xt = molski delež topljenca
Nt = število molov topljenca
Np = število molov topila
Molski delež topila (Xp)
Formula za molski delež topila (Xp), in sicer:

Informacije
Xp = molski delež topila
Nt = število molov topljenca
Np = število molov topila
Vsota molskih deležev topljenca in topila je 1
Xt + Xp = 1
Primeri težav z molalnostjo in rešitev
Problem 1
Kolikšna je molalnost raztopine, ki vsebuje 4 g NaOH (Ar Na = 23 g/mol, Ar O = 16 g/mol in Ar H = 1 g/mol), raztopljenega v 250 g vode?
Dokončanje:
Je znan:
masa NaOH = 4 gr
ArNa = 23 g/mol
ArO = 16 g/mol
ArH = 1 g/mol
masa vode = 250 gr = 0,25 kg
Vprašano: m = ?
odgovor:
Gospod. NaOH = 40 gr/mol
število molov NaOH = masa/Mr
število molov NaOH = 4 gr/(40 gr/mol)
število molov NaOH = 0,1 mol
m = število molov/p
m = 0,1 mol/0,25 kg
m = 0,4 m
Problem 2
Kakšna je molalnost 37-odstotne (m/m) raztopine HCl? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol)
Dokončanje:
Je znan:
masa HCl = 37%
ArH = 1 g/mol
ArCl = 35,5 g/mol
Vprašano: m = ?
odgovor:
Gospod. HCl = 36,5 g/mol
Recimo, da je masa raztopine 100 gramov, potem je masa HCl:
HCl masa = 37 % x 100 gr
masa HCl = 37 gr
masa topila = masa raztopine – masa HCl
masa topila = 100 gr – 37 gr
masa topila = 63 gr = 0,063 kg
število molov HCl = masa/Mr
število molov HCl = 37 g /(36,5 g/mol)
število molov HCl = 1,01 mola
m = število molov/masa topila
m = 1,01 mol/0,063 kg
m = 16,03 m
Problem 3
Določite molalnost raztopine, pripravljene tako, da raztopite 12 gramov sečnine CO(NH2)2 v 250 gramih vode.
Dokončanje:
Je znan:
masa sečnine = 12 gr
Mr Urea = 60 g/mol
masa topila = 250 gr = 0,25 kg
Vprašano: m = ?
Oglaševanje
odgovor:
število molov sečnine = masa/g
število molov sečnine = 12 g /(60 g/mol)
število molov sečnine = 0,2 mola
m = število molov/masa topila
m = 0,2 mol/0,25 kg
m = 0,8 m
Problem 4
Kakšna je molalnost alkoholne raztopine, ki vsebuje 23 masnih % etanola (Mr = 46)?
odgovor:
Je znan:
masa etanola = 23 %
Mr etanol = 46 g/mol
Vprašano: m = ?
Dokončanje:
na primer masa alkoholne raztopine je 100 gramov, masa etanola je:
masa etanola = 23 % x 100 gr
masa etanola = 23 gr
masa topila = masa raztopine – masa etanola
masa topila = 100 gr – 23 gr
masa topila = 77 gr = 0,077 kg
število molov etanola = masa/g
število molov etanola = 23 g /(46 g/mol)
število molov etanola = 0,5 mol
m = število molov/masa topila
m = 0,5 mol/0,077 kg
m = 6,49 m
Problem 5
Izračunajte koncentracijo (masni %) glukoze v 2 molni raztopini glukoze.
Dokončanje:
Je znan:
m = 2 molal = 2 mol/kg = 0,002 mol/gr
Mr glukoza = 180 gr/mol
vprašal: masa glukoze (%) = ?
odgovor:
molov glukoze = masa/g
mol glukoze = masa glukoze/(180 g/mol)
molov glukoze = masa glukoze x 0,005 mol/gr
Nadomestite mole glukoze v naslednjo enačbo:
m = mol glukoze/masa topila
0,002 = masa glukoze x 0,005/masa topila
o, oo2/o, oo5 = masa glukoze/masa topila
2/5 = masa glukoze/masa topila
Torej je masno razmerje glukoze: masa topila = 2:5, medtem ko je masno razmerje glukoze: masa raztopine = 2:7.
Torej,
% mase glukoze = (masa glukoze/masa raztopine) x 100 %
masni % glukoze = (2/7) x 100 %
% mase glukoze = 28,57 %
Problem 6
Kolikšna je molalnost raztopine, ki vsebuje 8 g NaOH (Ar Na = 23 g/mol, Ar O = 16 g/mol in Ar H = 1 g/mol), raztopljenega v 250 g vode?
Diskusija
Je znan:
Masa NaOH = 8 gr
ArNa = 23 g/mol
ArO = 16 g/mol
ArH = 1 g/mol
masa vode = 250 gr = 0,25 kg
Išče se: Molalnost (m)….?
odgovor:
Gospod. NaOH = 40 gr/mol
Število molov NaOH = masa/Mr
Število molov NaOH = 8 gr/(40 gr/mol)
Število molov NaOH = 0,2 mol
m = število molov/p
m = 0,2 mol/0,25 kg
m = 0,8 m
Problem 6
Določite molalnost raztopine, pripravljene tako, da raztopite 15 gramov sečnine CO(NH2)2 v 250 gramih vode.
Diskusija
Je znan:
Masa sečnine = 15 gr
Mr Urea = 60 g/mol
Masa topila = 250 gr = 0,25 kg
Išče se: Molalnost (m)…. ?
odgovor:
Število molov sečnine = masa/g
Skupni mol sečnine = 15 g / 60 g/mol
Število molov sečnine = 0,25 mol
m = število molov/masa topila
m = 0,25 mol / 0,25 kg
m = 1 m
Problem 7
Kakšna je molalnost 37-odstotne (m/m) raztopine HCl? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol).
Diskusija
Je znan:
masa HCl = 37%
ArH = 1 g/mol
ArCl = 35,5 g/mol
Išče se: Molalnost (m)…?
odgovor:
Gospod. HCl = 36,5 g/mol
Recimo, da je masa raztopine 100 gramov, potem je masa HCl:
HCl masa = 37 % x 100 gr
masa HCl = 37 gr
masa topila = masa raztopine – masa HCl
masa topila = 100 gr – 37 gr
masa topila = 63 gr = 0,063 kg
število molov HCl = masa/Mr
število molov HCl = 37 g /(36,5 g/mol)
število molov HCl = 1,01 mola
m = število molov/masa topila
m = 1,01 mol/0,063 kg
m = 16,03 m

Problem 8
Določite količino (v gramih) NaOH, ki jo morate raztopiti v 1 litru vode (voda = 1,00 g/mL), da dobite 0,25 m NaOH.
Diskusija
Je znan:
1 L vode = 1000 ml = 1000 g (ker je ρ vode = 1,00 g/mL)
mNaOH = 0,25 m
Mr NaOh = 40
Vprašano: gr…?
odgovor:
mNaOH = gr / Mr x 1.000 / P
0,25 = gr/40 x 1000/1000
0,25 = g/40
g = 0,25 x 40
g = 10 gramov
Torej je potrebna količina NaOH 10 gramov.
Problem 9
Ugotovite, koliko mL vode potrebujete za raztapljanje 4,9 grama H2SO4, katere koncentracija je 0,25 M (Ar H = 1; S = 32; O = 16)!
Diskusija
Je znan:
mH2SO4 = 0,25
Mr H2SO4 = 98
gr = 4,9 grama
Vprašano :p???
odgovor:
m = gr/Mr x 1.000/P
0,25 = 4,9/98 x 1.000/str
p = 20 gramov (20 ml)
Torej je prostornina vode 20 ml.
Problem 10
Kakšna masa vode je potrebna za pripravo 1,2 m raztopine z 0,6 mol NaCl?
Diskusija
molalnost (m) = 1,2 mm =
np
1,2 =
0,6p
P=
0,61,2
= 0,5 kg
Torej je potrebna masa vode (masa topila) 0,5 kg
Problem 11
Recimo, da sta 2 mola topljenca raztopljena v 1 litru topila, kakšna je molalnost?
Diskusija
raztopljeni mol (n) = 2 molm =
np
m =
21
= 2m
Izračunajte molalnost 25 gramov KBr (Mr = 119), raztopljenega v 750 ml čiste vode.
Diskusija
topljenec = 25 gramov
gospod = 119
topilo (P) = 750 mL = 750 gramov (ker je ρ vode = 1,00 g/mL) = 0,75 kgn =
raztopljeno snovgospod
n =
25119
= 0,21 mol
m =
np
m =
0,210,75
= 0,28 m
Tako pregled iz O znanju.co.id približno Primer problema molalnosti , upam, da lahko prispeva k vašemu vpogledu in znanju. Hvala za obisk in ne pozabite prebrati drugih člankov.
Seznam vsebine
Priporočilo:
- Celuloza je: definicija, vrsta, struktura, lastnosti in… Celuloza je: definicija, vrsta, struktura, lastnosti in funkcije - Celuloza je vlaknam podobna spojina in jo najdemo v zaščitnih celičnih stenah rastlin. Za boljše razumevanje bomo seveda razpravljali ...
- √ Opredelitev razširitve v dolžino, formulo, površino in prostornino snovi ... Definicija dolgega raztezanja, formule, površina in prostornina trdnih snovi - V tej razpravi bomo razložili dolgo raztezanje. Kar vključuje pojem dolge ekspanzije, formule dolge ekspanzije, površino, prostornino snovi ...
- Mere: definicija, pretvorba enot za dolžino, kako ... Merilna lestvica: definicija, pretvorba dolžinskih enot, uporaba in primeri vprašanj - Kaj je v kaj mislite z lestvico velikosti in kako jo uporabljati?, bo tokrat na znanje.co.id razpravljaj o tem...
- Kovalentne vezi: definicija, značilnosti, vrste, formule… Kovalentne vezi: definicija, značilnosti, vrste, kemijske formule in lastnosti spojin - Kaj je kovalentna vez? Ob tej priložnosti bo Seputarknowledge.co.id razpravljal o tem in seveda tudi o drugih stvareh pokrila. Pustiti…
- Okoljski govor: definicija, namen, značilnosti in… Okoljski govor: definicija, namen, značilnosti in primeri - Kako je strukturirano besedilo okoljskega govora? kaj je dobro in prav?, ob tej priložnosti bo Seputarknowledge.co.id razpravljal o tem in seveda o stvareh Katera…
- Formule stožcev, karakteristike, lastnosti, elementi in primeri problemov Formule stožca, značilnosti, lastnosti, elementi in primeri Težava - Kako izračunati površino in prostornino oblike cone space?, ob tej priložnosti bo Seputarknowledge.co.id razpravljal o tem in seveda o drugih stvareh Katera…
- Formula viskoznosti: definicija viskoznosti, koeficienta in… Formula viskoznosti: Definicija viskoznosti, koeficient in vplivni dejavniki - Kako je formula viskoznosti Viskoznost je meritev upora tekočine, ki se spremeni zaradi obremenitve ali pritisk. Ob tej priložnosti Seputarknowledge.co.id…
- Enota teže: definicija, pretvorbena lestvica in primeri… Enota za težo: definicija, pretvorbena lestvica in primer problema - Kaj je enota za težo?, ob tej priložnosti Glede znanja.co.id bo razpravljal o tem, vključno z razumevanjem in seveda tudi drugimi stvarmi pokrila. Pustiti…
- Vztrajnostni moment: definicija, faktorji, enačbe oblik… Vztrajnostni moment: definicija, dejavniki, enačbe v oblikah predmetov in primeri problemov - Kaj je mišljeno z vztrajnostnim momentom?, Ob tej priložnosti bo Se v zvezi z znanjem.co.id razpravljal o tem in seveda o zadeva…
- Enakomerno spreminjajoče se krožno gibanje: definicija, velikost… Enakomerno spreminjajoče se krožno gibanje: definicija, fizikalna količina, formule in primeri problemov - Kaj je gibanje Krožne spremembe redno in primeri? Ob tej priložnosti bo Seputarknowledge.co.id razpravljal o tem in seveda o...
- Nedoločen integral: definicija, formule, lastnosti in primeri… Nedoločen integral: definicija, formule, lastnosti in primeri problemov - Kaj pomeni nedoločen integral Seveda in kako izračunati matematične operacije? volja…
- Opredelitev učnih metod: značilnosti, namen, vrste in… Opredelitev učnih metod: Značilnosti, namen, vrste in razprava - Kaj pomeni metoda Učenje?, ob tej priložnosti bo Seputarknowledge.co.id razpravljal o tem in seveda o drugih stvareh Tudi…
- Kemijsko ravnovesje: definicija, zakoni, formule, primeri problemov Kemijsko ravnovesje: definicija, zakoni, formule, primeri težav - V tej razpravi bomo razložili o kemijskem ravnovesju, formulski zakon in opremljen s primeri kemijskega ravnovesja s popolno in...
- Kislinsko-bazične raztopine: definicija, kislinsko-bazična teorija, lastnosti in… Kislinsko-bazične raztopine: definicija, kislinsko-bazična teorija, lastnosti in vrste - Kislinske in bazične raztopine sta dve skupini kemičnih spojin, ki jih pogosto najdemo in uporabljamo v vsakdanjem življenju.
- Zgradite prostor – definicija, formule in razno… Zgradite prostor – definicija, formule in njegove različne vrste - Ob tej priložnosti bi radi ponovili matematično gradivo o geometrijskih oblikah, tako iz razumevanja kot drugih. Takoj se pogovorimo ...
- √ Kislo-bazični indikator: definicija, vrste in primeri Kislinsko-bazični indikatorji: definicija, vrste in primeri - Ob tej priložnosti bo Around Knowledge obravnaval kislinsko-bazične indikatorje. Kar v tej razpravi pojasnjuje pomen indikatorja kisline ...
- Boylov zakon: definicija, formule, aplikacije in primeri… Boylov zakon: definicija, formule, aplikacije in primeri problemov - V tej razpravi bomo razložili Boylov zakon. Kar vključuje pomen Boyleovega zakona, formulo Boyleovega zakona, uporabo ...
- Motivacijske kratke zgodbe: definicija, nasveti za pisanje in primeri Motivacijske kratke zgodbe: definicija, nasveti za pisanje in primeri - Kaj je motivacijska kratka zgodba?, naprej Ob tej priložnosti bo Seputarknowledge.co.id razpravljal o tem, ali gre za Kratko zgodbo o prijateljstvu in drugih stvareh. o tem. Pa poglejmo…
- Opredelitev tlaka: vrste tlaka, formule in primeri nalog Opredelitev tlaka: Vrste tlaka, formule in primeri nalog - Kaj je tlak? At Ob tej priložnosti bomo okoli znanja.co.id razpravljali o tem, kaj je pritisk in kaj so drugi elementi pokrila. Pa poglejmo…
- Dinamične tekočine: vrste, značilnosti, Bernoullijeva enačba, izreki… Dinamične tekočine: vrste, lastnosti, Bernoullijeva enačba, Toricellijev izrek, formule in primeri problemov - kaj je to dinamična tekočina in katere vrste? približno ...
- Gostota vode: definicija, formule in primeri Gostota vode: definicija, formule in primeri - Kakšna je gostota vode? Poglejmo skupaj…
- Opredelitev količine, enote, mere in primeri… Opredelitev količine, enote, meritve in primeri (popolno) - Pri osnovnih pojmih fizike smo se zagotovo seznanili z nečim, kar je povezano z vsakdanjim življenjem. Tako kot merjenje višine, tehtanje mase, merjenje širine, ...
- Primeri znanstvenih del: Funkcije in pravila jezika Primeri znanstvenih člankov: Funkcije in pravila jezika - Kateri so primeri dobrih in pravilnih oblik pisanja znanstvenih člankov? Pred tem je Seputar the knowledge.co.id razpravljal o znanstvenem delu: definicija, značilnosti, prednosti,…
- Primeri ploščatih oblik: Vrste, značilnosti in formule ploščatih oblik Primeri ravnih oblik: vrste, lastnosti in formule ravnih oblik - Kateri so primeri ravnih oblik?
- Vzorci vprašanj o telesni vzgoji za 11. razred (XI) SMA/MA/SMK, 1. in 2. semester Primeri vprašanj o telesni vzgoji za 11. razred (XI) za 1. in 2. semester SMA/MA/SMK (2019 in 2020) – ob tej priložnosti bo Seputarknowledge.co.id razpravljal o primerih vprašanj o telesni vzgoji za 11. razred z izbirnimi odgovori in esej ...
- Padavine so: 12 definicij po mnenju strokovnjakov, vrste,… Padavine so: 12 definicij glede na vrste strokovnjakov in dejavnike - V tej razpravi bo Around Knowledge razložil padavine. Padavine so podnebni dogodek, ki je naraven,...
- √ Opredelitev kemičnih spojin, lastnosti, vrst in nomenklature ... Opredelitev kemičnih spojin, značilnosti, vrste, popolna nomenklatura - V tej razpravi bomo razložili o kemičnih spojinah. Zajema definicijo, značilnosti, vrste in nomenklaturo kemičnih spojin z razpravo...
- Posamezne snovi so: definicija, elementi in spojine Posamezne snovi so: definicije, elementi in spojine - Kaj pomeni ena sama snov? Poglejmo skupaj razpravo ...
- Nagnjena ravnina: definicija, formule, mehanska prednost in… Poševna ravnina: definicija, formule, mehanske prednosti in primeri problemov - Kaj pomeni ravnina poševno in kako izračunati fiziko? naravno…
- Pretvorba enot: definicija, faktor, dolžina, masa, čas,… Pretvorba enot: definicija, faktor, dolžina, masa, čas, prostornina in tlak - Kaj je pretvorba enot?, Ob tej priložnosti bo Seputarknowledge.co.id razpravljal o tem, vključno z dejavniki, vrstami in seveda drugimi stvarmi Katera…
