Закон Бойля: определение, формулы, приложения, примеры задач
Закон Бойля: определение, формулы, приложения и примеры задач - В этой дискуссии мы объясним закон Бойля. Это включает понимание закона Бойля, формулы закона Бойля, применение закона Бойля и примеры вопросов из закона Бойля, которые обсуждаются полностью и легко. Для получения более подробной информации, пожалуйста, внимательно прочтите обзоры ниже.
Оглавление
-
Закон Бойля: определение, формулы, приложения и примеры задач
- Определение закона Бойля
- Формула закона Бойля
- Применение закона Бойля
- Пример закона Бойля
- Поделись этим:
- Похожие сообщения:
Закон Бойля: определение, формулы, приложения и примеры задач
Давайте сначала обсудим закон Бойля.
Определение закона Бойля
Закон Бойля - один из законов физики, в котором обсуждается взаимосвязь между давлением и объемом в газе. Роберт Бойль является первооткрывателем закона Бойля в том году (1627–1691), он провел исследование, чтобы узнать взаимосвязь между давлением и объемом газа при постоянной температуре. В ходе своего исследования Роберт Бойль обнаружил, что произведение давления и объема газа в замкнутом пространстве постоянно.
Согласно Википедии, другое определение закона Бойля - это один из многих законов химии и частный случай идеального закона химии. Если температура остается постоянной в замкнутой системе, закон Бойля описывает обратную зависимость между абсолютным давлением и объемом воздуха.
Закон Бойля, открытый Робертом Бойлем, изучает влияние давления на объем газа при постоянной температуре. Это утверждение Роберта Бойля называется законом Бойля, и оно гласит:
«При постоянной температуре давление газа в замкнутом пространстве обратно пропорционально его объему».
В повседневной жизни мы часто встречаем примеры инструментов, которые работают по закону Бойля, в том числе велосипедные насосы, шприцы и так далее.

Формула закона Бойля
Согласно закону Бойля это означает, что произведение давления и объема газа в замкнутом пространстве постоянно при постоянной температуре газа.
Приведенное выше утверждение, записанное в формуле, а именно:
P.V = C
Где C - фиксированное число (константа). Если давление изменится, изменится и количество газа, тогда формулу выше можно записать следующим образом:
P1. V1 = P2. V2
Читайте также:Момент инерции: определение, факторы, уравнения формы объектов и примеры задач
При условии:
P1 = начальное давление газа (атм. см рт. ст., Н / м2, Па)
P2 = конечное давление газа (атм, см рт. ст., Н / м2, Па)
V1 = исходный объем газа (м3, см3)
V2 = конечный объем газа (м3, см3)
Закон Бойля применяется только тогда, когда:
- Фиксированная температура газа или постоянная
- Газ в закрытом помещении
- Никакой химической реакции
- Без изменений газообразного состояния
Применение закона Бойля
Применение закона Бойля основано на принципе работы насоса. Насос - это устройство, используемое для транспортировки газа / жидкости. По такому принципу работы насос делится на две части: всасывающий и нагнетательный.
После вдоха количество воздуха в насосе увеличивается, и воздух не может попасть в шину, потому что воздух должен поступать через клапан (вентиляционное отверстие), сделанный из резины.
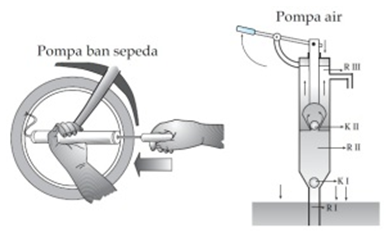
Если нажать на впускное отверстие, количество воздуха в насосе уменьшится, и из-за увеличения давления воздух может попасть в шину через вентиляционную трубку. Аналогичные устройства, использующие закон Бойля, - это шприцы, пипетки, нагнетательные насосы и водяные насосы.
Пример закона Бойля
Ниже приведены примеры проблем, связанных с законом Бойля:
1. В закрытой камере находится газ объемом 200 мл. Если давление в помещении 60см рт.ст., то рассчитать давление газа в помещении объемом 150 мл?
Решение:
Известен:
V1 = 200 мл
P1 = 60 см рт. Ст.
V2 = 150 мл
Спросил: P2…?
Отвечать:
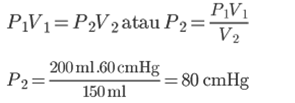
Согласно закону Бойля, давление газа в помещении объемом 250 мл составляет 80 см рт. Ст.
2. В закрытом помещении объемом 0,2 м3, заполненном газом, если давление увеличить до 80 000 Па?
Решение:
Известен:
P1 = 60 000 Па
V1 = 0,2 м3
P2 = 80 000 Па Спрошено: V2…?
Отвечать:
P1V1=P2 V2
V2 = (P1 V1): P2
V2 = (60 000 x 0,2): 80 000
V2 = 1,2/8
V2 = 0,15 м3 Таким образом, объем газа становится 0,15 м3
3. О законе Бойля, стр. V = k, k имеет размеры ...
А. Мощность
Б. Усилие
С. Линейный импульс
Д. Температура
Э. Постоянная пружины
Ответ: B
Обсуждение:
Известен: В.п = k
Спросил: k = …?
Отвечать:
п. V = k
к = р. V = (м³)
k = Нм = Джоуль
Джоуль - это единица работы. Итак, k имеет размерность усилия.
4. Что из следующего не является условием для выполнения закона Бойля:
Читайте также:Клонирование - это: определение, типы, преимущества и примеры
А. Фиксированная температура
Б. Фиксированный объем и давление
С. Никакой химической реакции не происходит
Д. Газ в закрытом помещении
Э. Состояние газа не меняется
Ответ: B
Обсуждение:
Закон Бойля применяется только при определенных условиях, таких как постоянная температура газа, газ в замкнутом пространстве, отсутствие химической реакции и отсутствие изменения газообразного состояния.
5. В закрытом контейнере находится газ, который расширяется так, что его объем увеличивается в 2 раза по сравнению с его начальным объемом (V = начальный объем, P = начальное давление). Давление газа изменится на ...
Обсуждение
Известен :
Начальное давление (P1) = п
Начальный объем (V1) = V
Окончательный объем (V2) = 2 В
Требуется: финальное давление (P2)
Отвечать:
P1 V1 = P2 V2
P V = P2 (2 В)
P = P2 (2)
P2 = P / 2 = п
Давление газа изменяется в разы по сравнению с начальным давлением.
6. В закрытом баллоне находится газ с давлением 2 атм и объемом 1 литр. Если давление газа изменится до 4 атм, объем газа будет ...
Обсуждение
Известен :
Начальное давление (P1) = 2 атм = 2 x 105 Паскалей
Конечное давление (P2) = 4 атм = 4 x 105 Паскалей
Начальный объем (V1) = 1 литр = 1 дм3 = 1 x 10-3 м3
Разыскивается: финальный том (V2)
Отвечать:
P1 V1 = P2 V2
(2 х 105) (1 х 10-3) = (4 х 105) V2
(1) (1 x 10-3) = (2) V2
1 х 10-3 = (2) V2
V2 = х 10-3
V2 = 0,5 x 10-3 м3 = 0,5 дм3 = 0,5 литра
7. В замкнутом пространстве находится газ объемом 200 мл. Что делать, если давление в комнате составляет 60 см рт. Ст., Поэтому рассчитайте давление газа в комнате, объем которой составляет 150 мл?
Решение:
Известен:
V1 = 200 мл
V2 = 150 мл
P1 = 60 см рт. Ст.
Спросил: P2 =…?
Отвечать:
P1. V1 = P2. V2
60 см рт. Ст. 20 мл = P2. 15 мл
P2 = 1200 см рт. Ст. / 15
P2 = 80 см рт. Ст.
Таким образом было объяснено о Закон Бойля: определение, формулы, приложения и примеры задач, надеюсь, может добавить к вашему пониманию и знаниям. Спасибо за посещение и не забывайте читать другие статьи.
