ラザフォード原子、その長所と短所を理解する
ラザフォード原子、長所と短所を理解する -この機会に 知識について ラザフォードアトムについて説明します。 この議論では、ラザフォードの原子の意味、理論、長所と短所を簡潔かつ明確に説明しています。 詳細については、次の記事を参照してください。
目次
-
ラザフォード原子、長所と短所を理解する
- Atomを理解する
- アーナーストラザフォードの原子理論
-
アーナーストラザフォードの原子理論の長所と短所。
- アーナーストラザフォードの原子理論
- エルナーストラザフォードの原子理論の不利な点
- これを共有:
- 関連記事:
ラザフォード原子、長所と短所を理解する
原子内の電子は、電磁力によって原子核に結合することができます。 そのような原子のいくつかのセットから、互いに関連することもでき、分子を形成することもできます。
同じ数の陽子と電子を含む原子は中性であり、次に 陽子または電子の数が異なると、正または負になり、イオンと呼ばれることがよくあります。
これらの原子は、原子核に含まれる陽子と中性子の数に基づいてグループ化されます。 原子内の陽子の数は原子の化学元素を決定し、中性子の数は特定の元素の同位体を決定します。
Atomを理解する
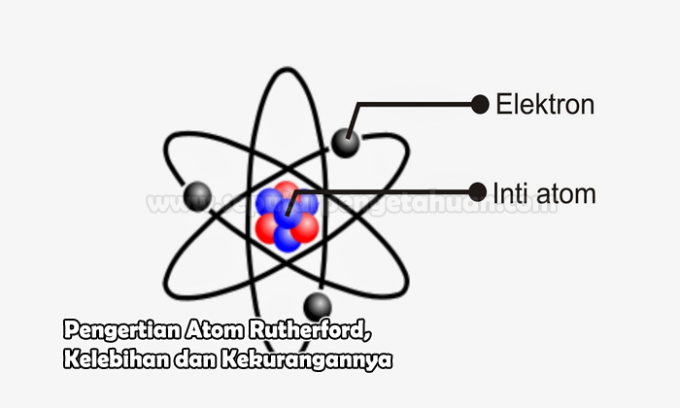
この原子は物質の基本単位であり、原子核とそれを取り囲む負に帯電した電子の雲で構成されています。 この原子の核は、正に帯電した陽子、または中性の電荷を持つ中性子で構成されています。
アーナーストラザフォードの原子理論
ジョン・ドルトンの原子理論が反駁され、後にJjによって修正された後。 トムソンは、原子はレーズンパンのようなものだと主張した。 それから、トムソムの原子理論の真実を否定するのはラザフォードの番でした。
また読む:進行波:定義、プロパティ、式、および問題の例
当時、ラザフォードは、原子には中心核がある、または負電荷を持つ電子の雲に囲まれた核と呼ばれることが多いと述べました。
ラザフォードの原子理論は、ガイガー・マースデン実験としてよく知られているアルファ粒子に金板の原子核を衝突させる実験に基づいていました。 その時、ラザフォードは放射性元素によって放出されたアルファ粒子による金原子の衝撃のための実験計画を起草するでしょう。
放射性光線の一部が反射、偏向、または転送されていることがわかります。 次にラザフォードは、アルファ粒子が原子核に当たると説明した。 次に、アルファ粒子のたわみまたは反射を引き起こす衝突が発生します。 これは、原子核に集中している原子の質量と電荷によるものです。
次に、ラザフォードは、原子核の電荷がSMA /原子質量単位の原子質量に比例することを示唆しました。 電子雲に当たるアルファ粒子は、偏向または反射されません。
これらの実験を通しての彼の理解の結果から、ErnerstRutherfordは最終的に次のように結論付けました。
- 原子の体積の大部分は真空です。
- 原子量は原子核(原子核)に集中します。
- 原子電荷は、かなり小さな体積で原子の中心に集中することができます。
- 電荷の倍数は原子量に比例します。
彼の声明によってE。 ラザフォードは、原子がレーズンパンのようではなかったことを否定することができました。 むしろ、それは太陽を周回する惑星の配置のようなものです。 太陽が正に帯電した中心核(原子核)または負に帯電した惑星の配置に例えられる場所。
したがって、ダルトンとトムソンの原子理論には長所と短所があります。 原子理論E。 ラザフォードには長所と短所があります。 以下は、原子理論Eの長所と短所です。 ラザフォード。
また読む:温度測定器、機能、種類、作業方法の理解(完全)
アーナーストラザフォードの原子理論の長所と短所。
ErnerstRutherfordの原子理論の長所と短所は次のとおりです。
アーナーストラザフォードの原子理論
- 原子の構造を説明できるように理解するのは非常に複雑です。
- 原子核の周りの電子軌道の形を説明することができます。
- 原子核の周りの電子の動きを説明できます。
エルナーストラザフォードの原子理論の不利な点
- ラザフォードの原子モデルでは、電子がどこにあるのか、また電子がこれらの原子の周りをどのように回転するのかを説明できていません。
- これらの電子は移動するとエネルギーを放出する可能性があるため、原子エネルギーは不安定になります。
- 水素原子(H)の線スペクトルを説明できません。
これはについての説明です ラザフォード原子、長所と短所を理解する. うまくいけば、それが有用であり、あなたの洞察に追加することができます。 ありがとうございました。
