Esempio di problema di molalità: frazione molare, formula e soluzione
Esempio di problema di molalità: frazione molare, formula e soluzione – In questa occasione Informazioni su knowledge.co.id discuterà la molalità con diversi esempi di domande e ovviamente su altre cose che la riguardano. Diamo un'occhiata alla discussione insieme nell'articolo qui sotto per capirlo meglio.
Esempio di problema di molalità: frazione molare, formula e soluzione
La molalità o concentrazione molare è una misura della concentrazione di un soluto in una soluzione in termini di quantità di sostanza in una certa massa del solvente. Questo è diverso dalla definizione di molarità che si basa su un certo volume di soluzione.
L'unità comune di molalità in chimica è mol/kg. Una soluzione con una concentrazione di 1 mol/kg è anche talvolta espressa come 1 molale. Il termine molalità è formato in analogia alla molarità che è la concentrazione molare di una soluzione.
La molalità di una soluzione può essere testata aggiungendo del solvente. Più semplicemente, la Molalità (m) di una soluzione è data dalle moli di soluto divise per i chilogrammi di solvente. La molalità o molalità è la concentrazione di una soluzione che indica il numero di moli (n) di soluto in 1 kg o 1000 grammi di solvente.
La differenza tra molalità e molarità è che se la molalità è molalità o concentrazione molare (m) esprime il numero di moli soluto in 1000 grammi di solvente mentre la molarità è una dichiarazione del numero di moli di soluto in ogni litro soluzione. La molarità è rappresentata dalla notazione M e le unità sono moli/litro.
Formula di molalità
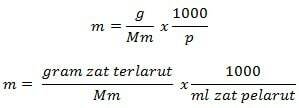
Informazione
m = molalità (mol/kg)
g = grammi di soluto (g)
Mm = massa molare della sostanza (g/mol)
P = massa di solvente (g)
Rapporto di molalità con percentuale di massa
La percentuale di massa è un'unità di concentrazione comunemente usata nelle soluzioni chimiche. Esempi di soluzioni che possiamo trovare tutti i giorni sono la soluzione alcolica al 75% e la soluzione di acido acetico al 24%. La percentuale di massa è il numero di grammi di soluto in 100 grammi di massa della soluzione. L'equazione che mostra il calcolo della percentuale di massa è la seguente:

Relazione molalità con molarità
La molarità esprime il numero di moli di soluto in un litro di soluzione. La molarità può essere convertita in molalità convertendo il volume della soluzione nella massa della soluzione. La conversione del volume in massa richiede dati sulla densità della soluzione (p), che possono essere formulati come segue:

Frazione molare
La frazione molare è una misura della concentrazione di una soluzione che esprime il rapporto tra il numero di moli in una parte di una sostanza e il numero totale di moli presenti nei componenti della soluzione. La frazione molare è divisa in 2 parti:
Frazione molare del soluto (Xt)
La formula per la frazione molare del soluto (Xt), vale a dire:

Informazione:
Xt = frazione molare del soluto
Nt = numero di moli di soluto
Np = numero di moli di solvente
Frazione molare del solvente (Xp)
La formula per la frazione molare del solvente (Xp), vale a dire:

Informazione
Xp = frazione molare del solvente
Nt = numero di moli di soluto
Np = numero di moli di solvente
La somma delle frazioni molari di soluto e solvente è 1
Xt + Xp = 1
Esempi di problemi di molalità e soluzioni
Problema 1
Qual è la molalità di una soluzione contenente 4 g di NaOH (Ar Na = 23 g/mol, Ar O = 16 g/mol e Ar H = 1 g/mol) sciolti in 250 g di acqua?
Completamento:
È conosciuto:
massa di NaOH = 4 gr
ArNa = 23 gr/mol
ArO = 16 g/mol
ArH = 1 gr/mol
massa d'acqua = 250 gr = 0,25 kg
Alla domanda: m = ?
Risposta:
Sig. NaOH = 40 gr/mol
numero di moli di NaOH = massa/Mr
numero di moli di NaOH = 4 gr/(40 gr/mol)
numero di moli di NaOH = 0,1 mol
m = numero di moli/p
m = 0,1 mol/0,25 kg
m = 0,4 m
Problema 2
Qual è la molalità di una soluzione di HCl al 37% (p/p)? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol)
Completamento:
È conosciuto:
massa di HCl = 37%
Ar H = 1 g/mol
ArCl = 35,5 g/mol
Alla domanda: m = ?
Risposta:
Sig. HCl = 36,5 gr/mol
supponiamo che la massa della soluzione sia 100 grammi allora la massa di HCl è:
Massa HCl = 37% x 100 gr
massa di HCl = 37 gr
massa di solvente = massa di soluzione – massa di HCl
massa di solvente = 100 gr – 37 gr
massa di solvente = 63 gr = 0,063 kg
numero di moli di HCl = massa/Mr
numero di moli di HCl = 37 gr /(36,5 gr/mol)
numero di moli di HCl = 1,01 moli
m = numero di moli/massa di solvente
m = 1,01 moli/0,063 kg
m = 16,03 m
Problema 3
Determinare la molalità della soluzione preparata sciogliendo 12 grammi di urea CO(NH2)2 in 250 grammi di acqua.
Completamento:
È conosciuto:
massa di urea = 12 gr
Signor Urea = 60 g/mol
massa di solvente = 250 gr = 0,25 kg
Alla domanda: m = ?
Annuncio
Risposta:
numero di moli di Urea = massa/Mr
numero di moli di Urea = 12 gr /(60 g/mol)
numero di moli di Urea = 0,2 moli
m = numero di moli/massa di solvente
m = 0,2 mol/0,25 kg
m = 0,8 m
Problema 4
Qual è la molalità di una soluzione alcolica contenente il 23% in massa di etanolo (Mr = 46)?
Risposta:
È conosciuto:
massa di etanolo = 23%
Mr etanolo = 46 g/mol
Alla domanda: m = ?
Completamento:
ad esempio la massa della soluzione alcolica è di 100 grammi, la massa dell'etanolo è:
massa di etanolo = 23% x 100 gr
massa di etanolo = 23 gr
massa di solvente = massa di soluzione – massa di etanolo
massa di solvente = 100 gr – 23 gr
massa di solvente = 77 gr = 0,077 kg
numero di moli di etanolo = massa/Mr
numero di moli di etanolo = 23 gr /(46 g/mol)
numero di moli di etanolo = 0,5 mol
m = numero di moli/massa di solvente
m = 0,5 mol/0,077 kg
m = 6,49 m
Problema 5
Calcolare la concentrazione (% in massa) di glucosio in una soluzione di glucosio 2 molare.
Completamento:
È conosciuto:
m = 2 molali = 2 mol/kg = 0,002 mol/gr
Signor glucosio = 180 gr/mol
Chiesto: massa di glucosio (%) = ?
Risposta:
moli di glucosio = massa/Mr
moli di glucosio = massa di glucosio/(180 g/mol)
moli di glucosio = massa di glucosio x 0,005 mol/gr
Sostituisci le moli di glucosio nella seguente equazione:
m = moli di glucosio/massa di solvente
0,002= massa di glucosio x 0,005/massa di solvente
o, oo2/o, oo5 = massa di glucosio/massa di solvente
2/5 = massa di glucosio/massa di solvente
Quindi il rapporto di massa del glucosio: massa del solvente = 2:5, mentre il rapporto di massa del glucosio: massa della soluzione = 2:7.
COSÌ,
% massa di glucosio = (massa di glucosio/massa di soluzione) x100%
% in massa di glucosio = (2/7) x 100%
% massa di glucosio = 28,57 %
Problema 6
Qual è la molalità di una soluzione contenente 8 g di NaOH (Ar Na = 23 g/mol, Ar O = 16 g/mol e Ar H = 1 g/mol) sciolti in 250 g di acqua?
Discussione
È conosciuto:
Massa di NaOH = 8 gr
ArNa = 23 gr/mol
ArO = 16 g/mol
ArH = 1 gr/mol
massa d'acqua = 250 gr = 0,25 kg
Ricercato: Molalità (m)….?
Risposta:
Sig. NaOH = 40 gr/mol
Il numero di moli di NaOH = massa/Mr
Numero di moli di NaOH = 8 gr/(40 gr/mol)
Il numero di moli di NaOH = 0,2 mol
m = numero di moli/p
m = 0,2 mol/0,25 kg
m = 0,8 m
Problema 6
Determinare la molalità della soluzione preparata sciogliendo 15 grammi di urea CO(NH2)2 in 250 grammi di acqua.
Discussione
È conosciuto:
Massa di urea = 15 gr
Signor Urea = 60 g/mol
Massa solvente = 250 gr = 0,25 kg
Ricercato: Molalità (m)…. ?
Risposta:
Numero di moli di Urea = massa/Mr
Moli totali di Urea = 15 gr / 60 g/mol
Il numero di moli di urea = 0,25 mol
m = numero di moli/massa di solvente
m = 0,25 mol/0,25 kg
m = 1 m
Problema 7
Qual è la molalità di una soluzione di HCl al 37% (p/p)? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol).
Discussione
È conosciuto:
massa di HCl = 37%
Ar H = 1 g/mol
ArCl = 35,5 g/mol
Ricercato: Molalità (m)???
Risposta:
Sig. HCl = 36,5 gr/mol
Supponiamo che la massa della soluzione sia di 100 grammi, quindi la massa di HCl è:
Massa HCl = 37% x 100 gr
massa di HCl = 37 gr
massa di solvente = massa di soluzione – massa di HCl
massa di solvente = 100 gr – 37 gr
massa di solvente = 63 gr = 0,063 kg
numero di moli di HCl = massa/Mr
numero di moli di HCl = 37 gr /(36,5 gr/mol)
numero di moli di HCl = 1,01 moli
m = numero di moli/massa di solvente
m = 1,01 moli/0,063 kg
m = 16,03 m

Problema 8
Determinare la quantità (grammi) di NaOH che deve essere sciolta in 1 litro di acqua (acqua = 1,00 g/mL) per ottenere 0,25 m NaOH.
Discussione
È conosciuto:
1 L di acqua = 1000 mL = 1000 g (poiché ρ di acqua = 1,00 g/mL)
mNaOH = 0,25 micron
Signor NaOh = 40
Alla domanda: gr???
Risposta:
mNaOH = gr/Mr x 1.000/P
0,25 = gr/40 x 1.000/1.000
0,25 = g/40
g = 0,25 x 40
g = 10 grammi
Quindi, la quantità di NaOH necessaria è di 10 grammi.
Problema 9
Determina quanti mL di acqua sono necessari per sciogliere 4,9 grammi di H2SO4 la cui concentrazione è 0,25 M (Ar H = 1; S = 32; O=16)!
Discussione
È conosciuto:
mH2SO4 = 0,25
Signor H2SO4 = 98
gr = 4,9 grammi
Chiesto: p???
Risposta:
m = gr/Mr x 1.000/P
0,25 = 4,9/98 x 1.000/p
p = 20 grammi (20 ml)
Quindi, il volume dell'acqua è di 20 ml.
Problema 10
Quale massa d'acqua è necessaria per preparare una soluzione di 1,2 m usando 0,6 mol di NaCl?
Discussione
molalità (m) = 1,2 mm =
NP
1,2 =
0,6P
P=
0,61,2
= 0,5kg
Quindi la massa d'acqua (massa di solvente) richiesta è di 0,5 kg
Problema 11
Supponiamo che ci siano 2 moli di soluto disciolte in 1 litro di solvente, qual è la molalità?
Discussione
moli disciolte (n) = 2 molm =
NP
m =
21
= 2 m
Calcolare la molalità di 25 grammi di KBr (Mr = 119) sciolti in 750 mL di acqua pura.
Discussione
soluto = 25 grammi
Signor = 119
solvente (P) = 750 mL = 750 grammi (poiché ρ di acqua = 1,00 g/mL) = 0,75 kgn =
sostanza discioltaSig
n =
25119
= 0,21 moli
m =
NP
m =
0,210,75
= 0,28 mt
Così la recensione di Informazioni su knowledge.co.id Di Esempio di un problema di molalità , si spera che possa aggiungere alla tua intuizione e conoscenza. Grazie per la visita e non dimenticare di leggere altri articoli.
Lista dei contenuti
Raccomandazione:
- La cellulosa è: definizione, tipo, struttura, proprietà e... La cellulosa è: definizione, tipo, struttura, proprietà e funzioni - La cellulosa è un composto simile alla fibra e si trova nelle pareti cellulari protettive delle piante. Per capire meglio, ovviamente discuteremo...
- √ Definizione di espansione in lunghezza, formula, area e volume della sostanza… Definizione di espansione lunga, formule, area e volume dei solidi - In questa discussione spiegheremo l'espansione lunga. Che include la nozione di lunga espansione, formule di lunga espansione, area, volume di materia...
- Misure: definizione, conversione unità di lunghezza, come... Scala di misurazione: definizione, conversione delle unità di lunghezza, modalità d'uso e domande di esempio - Cosa c'è dentro cosa intendi per scala di dimensioni e come usarla?, questa volta lo farà knowledge.co.id discuterne...
- Legami covalenti: definizione, caratteristiche, tipi, formule... Legami covalenti: definizione, caratteristiche, tipi, formule chimiche e proprietà dei composti - Cos'è un legame covalente? In questa occasione, Seputarknowledge.co.id ne parlerà e ovviamente anche di altre cose l'ha coperto. Permettere…
- Discorso ambientale: definizione, scopo, caratteristiche e... Discorso ambientale: definizione, scopo, caratteristiche ed esempi - Come è strutturato il testo del discorso ambientale? cosa è buono e giusto?, In questa occasione, Seputarknowledge.co.id ne discuterà e ovviamente le cose Quale…
- Formule del cono, caratteristiche, proprietà, elementi ed esempi di problemi Cono Formule, caratteristiche, proprietà, elementi ed esempi Problema - Come calcolare l'area e il volume di una forma cone space?, In questa occasione, Seputarknowledge.co.id ne parlerà e ovviamente di altre cose Quale…
- Formula della viscosità: definizione di viscosità, coefficiente e... Formula di viscosità: definizione di viscosità, coefficiente e fattori di influenza - Com'è la formula di viscosità La viscosità è una misura della resistenza di un fluido che viene modificata dallo stress o da pressione. In questa occasione, Seputarknowledge.co.id...
- Unità di peso: definizione, scala di conversione ed esempi... Unità di peso: definizione, scala di conversione e problema di esempio - Cos'è un'unità di peso?, In questa occasione About the knowledge.co.id ne discuterà, inclusa la comprensione e ovviamente anche altre cose l'ha coperto. Permettere…
- Momento d'inerzia: definizione, fattori, equazioni di forme... Momento di inerzia: definizione, fattori, equazioni in forme di oggetti e problemi di esempio - Cosa si intende con il momento di inerzia?, In questa occasione, Se per quanto riguarda la conoscenza.co.id ne discuterà e ovviamente su questione…
- Moto circolare che cambia uniformemente: definizione, grandezza... Moto circolare che cambia uniformemente: definizione, quantità fisica, formule ed esempi di problemi - Cos'è il movimento Modifiche circolari regolarmente ed esempi? In questa occasione, Seputarknowledge.co.id ne discuterà e ovviamente circa...
- Integrale indefinito: definizione, formule, proprietà ed esempi... Integrale indefinito: definizione, formule, proprietà ed esempi di problemi - Cosa si intende per integrale indefinito Certo e come calcolare le operazioni matematiche? Volere…
- Definizione dei metodi di apprendimento: caratteristiche, scopo, tipi e... Definizione dei metodi di apprendimento: caratteristiche, finalità, tipologie e discussione - Cosa si intende per metodo Imparare?, In questa occasione, Seputarknowledge.co.id ne parlerà e ovviamente di altre cose Anche…
- Equilibrio chimico: definizione, leggi, formule, problemi di esempio Equilibrio chimico: definizione, leggi, formule, problemi di esempio - In questa discussione spiegheremo sull'equilibrio chimico, legge sulla formula e corredato di esempi di equilibrio chimico con complete e...
- Soluzioni acido-base: definizione, teoria acido-base, proprietà e... Soluzioni acido-base: definizione, teoria acido-base, proprietà e tipi - Le soluzioni acide e basiche sono due gruppi di composti chimici che sono ampiamente trovati e utilizzati nella vita di tutti i giorni.
- Costruisci spazio: definizione, formule e vari ... Costruire lo spazio - Definizione, formule e vari tipi - In questa occasione, vorremmo rivedere il materiale matematico sulle forme geometriche, sia in termini di comprensione che in altri. Discutiamo subito...
- √ Indicatore acido-base: definizione, tipi ed esempi Indicatori acido-base: definizione, tipologie ed esempi - In questa occasione, Around Knowledge parlerà di indicatori acido-base. Che in questa discussione spiega il significato di indicatore acido...
- Legge di Boyle: definizione, formule, applicazioni ed esempi... Legge di Boyle: definizione, formule, applicazioni ed esempi di problemi - In questa discussione spiegheremo la legge di Boyle. Che include il significato della legge di Boyle, la formula della legge di Boyle, l'applicazione di...
- Racconti motivazionali: definizione, consigli di scrittura ed esempi Racconti motivazionali: definizione, suggerimenti per la scrittura ed esempi - Che cos'è un racconto motivazionale?, On In questa occasione, Seputarknowledge.co.id discuterà se si tratta del racconto breve dell'amicizia e di altre cose a proposito. Vediamo…
- Definizione di pressione: tipi di pressione, formule e problemi di esempio Definizione di pressione: tipi di pressione, formule ed esempi di problemi - Che cos'è la pressione? In questa occasione, attorno a knowledge.co.id, discuteremo cos'è la pressione e quali sono gli altri elementi l'ha coperto. Vediamo…
- Fluidi Dinamici: Tipi, Caratteristiche, Equazione di Bernoulli, Teoremi... Fluidi dinamici: tipi, proprietà, equazione di Bernoulli, teorema di Toricelli, formule ed esempi di problemi - Che cos'è fluidi dinamici e loro tipi? Di…
- Densità dell'acqua: definizione, formule ed esempi Densità dell'acqua: definizione, formule ed esempi - Qual è la densità dell'acqua? Vediamo insieme…
- Definizione di quantità, unità, misura ed esempi... Definizione di quantità, unità, misura ed esempi (completi) - Nei concetti fisici di base, sicuramente siamo stati introdotti a qualcosa relativo alla vita di tutti i giorni. Come misurare l'altezza, pesare la massa, misurare la larghezza,...
- Esempi di lavoro scientifico: funzioni e regole del linguaggio Esempi di articoli scientifici: funzioni e regole del linguaggio - Quali sono esempi di buone e corrette forme di scrittura di articoli scientifici? In precedenza, Seputar the knowledge.co.id ha discusso il lavoro scientifico: definizione, caratteristiche, vantaggi, ...
- Esempi di forme piatte: tipi, caratteristiche e formule delle forme piatte Esempi di forme piatte: tipi, proprietà e formule delle forme piatte - Quali sono gli esempi di forme piatte?
- Esempio di domande di educazione fisica per la classe 11 (XI) SMA/MA/SMK Semestre 1 e 2 Esempi di domande di educazione fisica per la classe 11 (XI) per SMA/MA/SMK semestre 1 e 2 (2019 e 2020) - In questa occasione, Seputarknowledge.co.id discuterà esempi di domande di educazione fisica per la classe 11 a scelta multipla e saggio ...
- Le precipitazioni sono: 12 definizioni secondo esperti, tipi, ... La precipitazione è: 12 definizioni secondo i tipi e i fattori degli esperti - In questa discussione, Around Knowledge spiegherà le precipitazioni. Le precipitazioni sono un evento climatico naturale,...
- √ Definizione di composti chimici, caratteristiche, tipi e nomenclatura... Definizione di composti chimici, caratteristiche, tipi, nomenclatura completa - In questa discussione spiegheremo i composti chimici. Copre la definizione, le caratteristiche, i tipi e la nomenclatura dei composti chimici con discussione...
- Le singole sostanze sono: definizione, elementi e composti Le singole sostanze sono: definizioni, elementi e composti - Cosa significa una singola sostanza? Rivediamo insieme la discussione...
- Piano inclinato: definizione, formule, vantaggio meccanico e... Piano obliquo: definizione, formule, vantaggi meccanici ed esempi di problemi - Cosa si intende per piano obliquo e come calcolare la fisica? naturalmente…
- Conversione di unità: definizione, fattore, lunghezza, massa, tempo,... Conversione di unità: definizione, fattore, lunghezza, massa, tempo, volume e pressione - Cos'è la conversione di unità?, In questa occasione, Seputarknowledge.co.id ne parlerà, inclusi fattori, tipi e ovviamente altre cose Quale…
