Esimerkki molaalisuusongelmasta: mooliosuus, kaava ja ratkaisu
Esimerkki molaalisuusongelmasta: mooliosuus, kaava ja ratkaisu - Tässä tapauksessa Tietoja osoitteesta know.co.id keskustelee molaalisuudesta useiden kysymysesimerkkien kera ja tietysti muista asioista, jotka myös kattavat sen. Katsotaanpa keskustelua yhdessä alla olevassa artikkelissa ymmärtääksemme sitä paremmin.
Esimerkki molaalisuusongelmasta: mooliosuus, kaava ja ratkaisu
Molaalisuus tai moolipitoisuus on liuenneen aineen pitoisuuden mitta liuoksessa aineen määränä tietyssä liuottimen massassa. Tämä eroaa molaarisuuden määritelmästä, joka perustuu tiettyyn liuoksen tilavuuteen.
Yleinen molaliteettiyksikkö kemiassa on mol/kg. Liuos, jonka pitoisuus on 1 mol/kg, ilmaistaan joskus myös 1 moolina. Termi molaarisuus muodostetaan analogisesti molaarisuuden kanssa, joka on liuoksen molaarinen pitoisuus.
Liuoksen molaalisuus voidaan testata lisäämällä liuotinta. Yksinkertaisemmin sanottuna liuoksen molaarisuus (m) on liuenneen aineen moolit jaettuna liuottimen kilogrammoilla. Molaalisuus tai molaalisuus on liuoksen pitoisuus, joka ilmoittaa liuenneen aineen moolimäärän (n) 1 kg: ssa tai 1000 grammassa liuotinta.
Ero molaalisuuden ja molaarisuuden välillä on se, että jos molaalisuus on molaalisuutta tai moolipitoisuus (m) ilmaisee moolien lukumäärän liuennutta ainetta 1000 grammassa liuotinta, kun taas molaarisuus on lausunto liuenneen aineen moolien määrästä jokaisessa litrassa ratkaisu. Molaarisuutta edustaa merkintä M ja yksiköt ovat moolia/litra.
Molality Formula
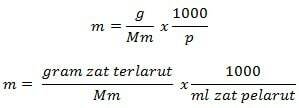
Tiedot
m = molaalisuus (mol/kg)
g = grammaa liuennutta ainetta (g)
Mm = aineen moolimassa (g/mol)
P = liuottimen massa (g)
Molaalisuussuhde massaprosenttiin
Massaprosentti on kemiallisissa liuoksissa yleisesti käytetty pitoisuusyksikkö. Esimerkkejä ratkaisuista, joita voimme löytää joka päivä, ovat 75-prosenttinen alkoholiliuos ja 24-prosenttinen etikkahappoliuos. Massaprosentti on liuenneen aineen gramman lukumäärä 100 grammassa liuosmassaa. Kaava, joka näyttää massaprosentin laskennan, on seuraava:

Suhteen molality ja molaarisuus
Molaarisuus ilmaisee liuenneen aineen moolien lukumäärän yhdessä litrassa liuosta. Molaarisuus voidaan muuntaa molaariseksi muuttamalla liuoksen tilavuus liuoksen massaksi. Tilavuuden muuntaminen massaksi vaatii tietoja liuoksen tiheydestä (p), joka voidaan muotoilla seuraavasti:

Mooliosuus
Mooliosuus on liuoksen pitoisuuden mitta, joka ilmaisee aineen osassa olevien moolien lukumäärän suhteessa liuoksen komponenteissa olevien moolien kokonaismäärään. Moolifraktio on jaettu 2 osaan:
Liuenneen aineen mooliosuus (Xt)
Kaava liuenneen aineen mooliosuudelle (Xt), nimittäin:

Tiedot:
Xt = liuenneen aineen mooliosuus
Nt = liuenneen aineen moolien lukumäärä
Np = liuottimen moolien lukumäärä
Liuottimen mooliosuus (Xp)
Kaava liuottimen mooliosuudelle (Xp), nimittäin:

Tiedot
Xp = liuottimen mooliosuus
Nt = liuenneen aineen moolien lukumäärä
Np = liuottimen moolien lukumäärä
Liuenneen aineen ja liuottimen mooliosien summa on 1
Xt + Xp = 1
Esimerkkejä molality-ongelmista ja -ratkaisuista
Ongelma 1
Mikä on liuoksen molaalisuus, joka sisältää 4 g NaOH: ta (Ar Na = 23 g/mol, Ar O = 16 g/mol ja Ar H = 1 g/mol) liuotettuna 250 g: aan vettä?
Valmistuminen:
Tunnetaan:
NaOH: n massa = 4 gr
ArNa = 23 g/mol
ArO = 16 g/mol
ArH = 1 g/mol
veden massa = 250 g = 0,25 kg
Kysyi: m = ?
Vastaus:
Herra. NaOH = 40 g/mol
NaOH-moolien lukumäärä = massa/Mr
NaOH-moolien lukumäärä = 4 g/(40 g/mol)
NaOH-moolien lukumäärä = 0,1 mol
m = moolien lukumäärä/p
m = 0,1 mol / 0,25 kg
m = 0,4 m
Ongelma 2
Mikä on 37-prosenttisen (w/w) HCl-liuoksen molaalisuus? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol)
Valmistuminen:
Tunnetaan:
HCl: n massa = 37 %
ArH = 1 g/mol
ArCl = 35,5 g/mol
Kysyi: m = ?
Vastaus:
Herra. HCl = 36,5 g/mol
oletetaan, että liuoksen massa on 100 grammaa, niin HCl: n massa on:
HCl-massa = 37 % x 100 gr
HCl: n massa = 37 gr
liuottimen massa = liuoksen massa – HCl: n massa
liuottimen massa = 100 gr – 37 gr
liuottimen massa = 63 g = 0,063 kg
HCl-moolien lukumäärä = massa/Mr
HCl-moolien määrä = 37 g /(36,5 g/mol)
HCl-moolien lukumäärä = 1,01 moolia
m = moolimäärä/liuottimen massa
m = 1,01 mol/0,063 kg
m = 16,03 m
Ongelma 3
Määritetään liuoksen molaalisuus, joka on valmistettu liuottamalla 12 grammaa urea CO(NH2)2:ta 250 grammaan vettä.
Valmistuminen:
Tunnetaan:
urean massa = 12 gr
Mr Urea = 60 g/mol
liuottimen massa = 250 g = 0,25 kg
Kysyi: m = ?
Mainos
Vastaus:
urean moolien lukumäärä = massa/Mr
Urean moolimäärä = 12 g /(60 g/mol)
urea-moolien määrä = 0,2 moolia
m = moolimäärä/liuottimen massa
m = 0,2 mol / 0,25 kg
m = 0,8 m
Ongelma 4
Mikä on 23 massaprosenttia etanolia (Mr = 46) sisältävän alkoholiliuoksen molaalisuus?
Vastaus:
Tunnetaan:
etanolin massa = 23 %
Mr etanoli = 46 g/mol
Kysyi: m = ?
Valmistuminen:
esimerkiksi alkoholiliuoksen massa on 100 grammaa, jolloin etanolin massa on:
etanolin massa = 23 % x 100 gr
etanolin massa = 23 gr
liuottimen massa = liuoksen massa – etanolin massa
liuottimen massa = 100 g – 23 gr
liuottimen massa = 77 g = 0,077 kg
etanolin moolimäärä = massa/Mr
etanolin moolimäärä = 23 g /(46 g/mol)
etanolin moolimäärä = 0,5 mol
m = moolimäärä/liuottimen massa
m = 0,5 mol/0,077 kg
m = 6,49 m
Ongelma 5
Laske glukoosin pitoisuus (massa-%) 2-molaarisessa glukoosiliuoksessa.
Valmistuminen:
Tunnetaan:
m = 2 mol/kg = 0,002 mol/gr
Mr glukoosi = 180 g/mol
Kysyi: glukoosin massa (%) = ?
Vastaus:
moolia glukoosia = massa/hr
moolia glukoosia = glukoosin massa/(180 g/mol)
moolia glukoosia = glukoosin massa x 0,005 mol/gr
Korvaa glukoosimoolit seuraavaan yhtälöön:
m = glukoosimooleja/liuottimen massa
0,002 = glukoosin massa x 0,005/liuottimen massa
o, oo2/o, oo5 = glukoosin massa/liuottimen massa
2/5 = glukoosin massa/liuottimen massa
Joten glukoosin ja liuottimen massasuhde = 2:5, kun taas glukoosin massasuhde liuoksen massa = 2:7.
Niin,
glukoosin massa % = (glukoosin massa/liuoksen massa) x100 %
glukoosin massaprosentti = (2/7) x 100 %
% glukoosimassa = 28,57 %
Ongelma 6
Mikä on liuoksen molaalisuus, joka sisältää 8 g NaOH: ta (Ar Na = 23 g/mol, Ar O = 16 g/mol ja Ar H = 1 g/mol) liuotettuna 250 g: aan vettä?
Keskustelu
Tunnetaan:
NaOH: n massa = 8 gr
ArNa = 23 g/mol
ArO = 16 g/mol
ArH = 1 g/mol
veden massa = 250 g = 0,25 kg
Vaihdetaan: Molality (m)….?
Vastaus:
Herra. NaOH = 40 g/mol
NaOH: n moolimäärä = massa/Mr
NaOH-moolimäärä = 8 g/(40 g/mol)
NaOH: n moolimäärä = 0,2 mol
m = moolien lukumäärä/p
m = 0,2 mol / 0,25 kg
m = 0,8 m
Ongelma 6
Määritetään liuoksen molaalisuus, joka valmistetaan liuottamalla 15 grammaa urea CO(NH2)2:ta 250 grammaan vettä.
Keskustelu
Tunnetaan:
Urean massa = 15 gr
Mr Urea = 60 g/mol
Liuottimen massa = 250 gr = 0,25 kg
Ostetaan: Molality (m)…. ?
Vastaus:
Urean moolien lukumäärä = massa/Mr
Urean kokonaismoolit = 15 g / 60 g/mol
Urean moolimäärä = 0,25 mol
m = moolimäärä/liuottimen massa
m = 0,25 mol / 0,25 kg
m = 1 m
Ongelma 7
Mikä on 37-prosenttisen (w/w) HCl-liuoksen molaalisuus? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol).
Keskustelu
Tunnetaan:
HCl: n massa = 37 %
ArH = 1 g/mol
ArCl = 35,5 g/mol
Ostetaan: Molality (m)…?
Vastaus:
Herra. HCl = 36,5 g/mol
Oletetaan, että liuoksen massa on 100 grammaa, niin HCl: n massa on:
HCl-massa = 37 % x 100 gr
HCl: n massa = 37 gr
liuottimen massa = liuoksen massa – HCl: n massa
liuottimen massa = 100 gr – 37 gr
liuottimen massa = 63 g = 0,063 kg
HCl-moolien lukumäärä = massa/Mr
HCl-moolien määrä = 37 g /(36,5 g/mol)
HCl-moolien lukumäärä = 1,01 moolia
m = moolimäärä/liuottimen massa
m = 1,01 mol/0,063 kg
m = 16,03 m

Ongelma 8
Määritä NaOH: n määrä (grammaa), joka on liuotettava 1 litraan vettä (vesi = 1,00 g/ml), jotta saadaan 0,25 m NaOH.
Keskustelu
Tunnetaan:
1 litra vettä = 1000 ml = 1000 g (koska ρ vettä = 1,00 g/ml)
mNaOH = 0,25 m
herra NaOh = 40
Kysyi: gr…?
Vastaus:
mNaOH = gr / herra x 1 000 / P
0,25 = gr / 40 x 1 000 / 1 000
0,25 = g/40
g = 0,25 x 40
g = 10 grammaa
Tarvittava NaOH-määrä on siis 10 grammaa.
Ongelma 9
Määritä, kuinka monta ml vettä tarvitaan liuottamaan 4,9 grammaa H2SO4:a, jonka pitoisuus on 0,25 M (Ar H = 1; S = 32; O = 16)!
Keskustelu
Tunnetaan:
mH2S04 = 0,25
Mr H2SO4 = 98
gr = 4,9 grammaa
Kysyi :p???
Vastaus:
m = gr/Mr x 1000/P
0,25 = 4,9/98 x 1 000/p
p = 20 grammaa (20 ml)
Joten veden tilavuus on 20 ml.
Ongelma 10
Kuinka paljon vettä tarvitaan 1,2 m liuoksen valmistamiseksi 0,6 mol NaCl: lla?
Keskustelu
molaliteetti (m) = 1,2 mm =
nP
1,2 =
0,6P
P=
0,61,2
= 0,5 kg
Tarvittava vesimassa (liuottimen massa) on siis 0,5 kg
Ongelma 11
Oletetaan, että 1 litrassa liuotinta on 2 moolia liuennutta ainetta, mikä on molaliteetti?
Keskustelu
liuenneet moolit (n) = 2 molm =
nP
m =
21
= 2 m
Laske 25 gramman KBr: n (Mr = 119) molaalisuus liuotettuna 750 ml: aan puhdasta vettä.
Keskustelu
liuennut aine = 25 grammaa
herra = 119
liuotin (P) = 750 ml = 750 grammaa (koska ρ vettä = 1,00 g/ml) = 0,75 kgn =
liuennut aineHerra
n =
25119
= 0,21 mol
m =
nP
m =
0,210,75
= 0,28 m
Näin ollen arvostelu alkaen Tietoja osoitteesta know.co.id noin Esimerkki molaalisuusongelmasta , toivottavasti voi lisätä ymmärrystäsi ja tietämystäsi. Kiitos vierailustasi ja älä unohda lukea muita artikkeleita.
Sisällysluettelo
Suositus:
- Selluloosa on: määritelmä, tyyppi, rakenne, ominaisuudet ja… Selluloosa on: Määritelmä, tyyppi, rakenne, ominaisuudet ja toiminnot - Selluloosa on kuidun kaltainen yhdiste, ja sitä löytyy kasvien suojaavista soluseinistä. Ymmärtääksemme paremmin, keskustelemme tietysti…
- √ Laajenemisen määritelmä pituus, kaava, pinta-ala ja aineen tilavuus… Pitkän laajenemisen määritelmä, kaavat, pinta-ala ja kiinteiden aineiden tilavuus - Tässä keskustelussa selitämme pitkästä laajenemisesta. Joka sisältää käsitteen pitkä laajeneminen, pitkät laajenemiskaavat, pinta-ala, aineen tilavuus...
- Toimenpiteet: määritelmä, pituusyksikön muunnos, miten… Mittausportaat: määritelmä, pituusyksiköiden muuntaminen, käyttö ja esimerkkikysymykset - mitä mitä tarkoitat kokotikkaalla ja miten niitä käytetään?, tällä kertaa tietämys.co.id keskustella siitä...
- Kovalenttiset sidokset: määritelmä, ominaisuudet, tyypit, kaavat… Kovalenttiset sidokset: Yhdisteiden määritelmä, ominaisuudet, tyypit, kemialliset kaavat ja ominaisuudet - Mikä on kovalenttinen sidos? Tällä kertaa Seputarknowledge.co.id keskustelee siitä ja tietysti myös muista asioista peitti sen. Antaa…
- Ympäristöpuhe: määritelmä, tarkoitus, ominaisuudet ja… Ympäristöpuhe: määritelmä, tarkoitus, ominaisuudet ja esimerkit - Miten ympäristöpuheen teksti on rakennettu? mikä on hyvää ja oikein?, Tällä kertaa Seputarknowledge.co.id keskustelee siitä ja tietysti asioista Mikä…
- Kartiokaavoja, ominaisuuksia, ominaisuuksia, elementtejä ja esimerkkejä ongelmista Kartiokaavat, ominaisuudet, ominaisuudet, elementit ja esimerkit Ongelma - Kuinka laskea muodon pinta-ala ja tilavuus kartiotila?, Tässä yhteydessä Seputarknowledge.co.id keskustelee siitä ja tietysti muista asioista Mikä…
- Viskositeettikaava: Viskositeetti, kerroin ja… Viskositeettikaava: viskositeetin määritelmä, kerroin ja vaikuttavat tekijät - kuinka viskositeettikaava on Viskositeetti on nesteen vastuksen mitta, joka muuttuu joko jännityksen tai vaikutuksen vaikutuksesta paine. Tässä yhteydessä Seputarknowledge.co.id…
- Painon yksikkö: määritelmä, muunnostikkaat ja esimerkkejä… Painon yksikkö: määritelmä, muunnostikkaat ja esimerkkiongelma – mikä on painoyksikkö?, tässä yhteydessä Knowledge.co.id: stä keskustellaan siitä, mukaan lukien ymmärrystä ja tietysti myös muista asioista peitti sen. Antaa…
- Hitausmomentti: määritelmä, tekijät, muotoyhtälöt… Hitausmomentti: määritelmä, tekijät, yhtälöt objektien muodoissa ja esimerkkitehtävät - mitä tarkoitetaan hitausmomentin kanssa?, tällä kertaa Se, joka koskee tietämystä.co.id: tä, keskustelee siitä ja tietysti asiaa…
- Tasaisesti muuttuva ympyräliike: määritelmä, suuruus… Tasaisesti muuttuva ympyräliike: määritelmä, fyysinen määrä, kaavat ja esimerkkejä ongelmista – mitä liike on Pyöreät muutokset säännöllisesti ja esimerkkejä? Tässä yhteydessä Seputarknowledge.co.id keskustelee siitä ja tietysti noin...
- Epämääräinen integraali: määritelmä, kaavat, ominaisuudet ja esimerkit… Epämääräinen integraali: määritelmä, kaavat, ominaisuudet ja esimerkkejä ongelmista - mitä tarkoittaa määrittelemätön integraali Tietenkin ja kuinka laskea matemaattiset operaatiot? tahtoa…
- Oppimismenetelmien määritelmä: ominaisuudet, tarkoitus, tyypit ja… Oppimismenetelmien määritelmä: ominaisuudet, tarkoitus, tyypit ja keskustelu – mitä menetelmällä tarkoitetaan Opitaanko?, Seputarknowledge.co.id keskustelee tällä kertaa siitä ja tietysti muista asioista Myös…
- Kemiallinen tasapaino: määritelmä, lait, kaavat, esimerkkiongelmat Kemiallinen tasapaino: määritelmä, lait, kaavat, esimerkkiongelmat - Tässä keskustelussa selitämme kemiallisesta tasapainosta, kaavan laista ja varustettu esimerkeillä kemiallisesta tasapainosta täydellisellä ja...
- Happo-emäsratkaisut: määritelmä, happo-emästeoria, ominaisuudet ja… Happo-emäsliuokset: määritelmä, happo-emäs-teoria, ominaisuudet ja tyypit - Happo- ja emäsliuokset ovat kaksi kemiallisten yhdisteiden ryhmää, joita löytyy ja käytetään laajalti jokapäiväisessä elämässä.
- Rakenna tilaa – määritelmät, kaavat ja erilaiset… Rakenna avaruus – määritelmät, kaavat ja sen eri tyypit – Tässä tilaisuudessa haluamme käydä läpi matemaattista materiaalia geometrisista muodoista, sekä ymmärryksestä että muista. Keskustellaan heti...
- √ Happo-emäs-indikaattori: määritelmä, tyypit ja esimerkit Happo-emäs-indikaattorit: Määritelmä, tyypit ja esimerkit - Tässä yhteydessä Around Knowledge käsittelee happo-emäs-indikaattoreita. Mikä tässä keskustelussa selittää happo-indikaattorin merkityksen...
- Boylen laki: määritelmä, kaavat, sovellukset ja esimerkit… Boylen laki: määritelmä, kaavat, sovellukset ja esimerkkejä ongelmista - Tässä keskustelussa selitämme Boylen laista. Joka sisältää Boylen lain merkityksen, Boylen lain kaavan, soveltamisen…
- Motivoivia novelleja: määritelmä, kirjoitusvinkkejä ja esimerkkejä Motivoivat novellit: määritelmä, kirjoitusvinkkejä ja esimerkkejä – mikä on motivoiva novelli? Tällä kertaa Seputarknowledge.co.id pohtii, onko se lyhyt tarina ystävyydestä ja muista asioista siitä. Katsotaan…
- Paineen määritelmä: painetyypit, kaavat ja esimerkkiongelmat Paineen määritelmä: painetyypit, kaavat ja esimerkkiongelmat - mikä on paine? Tässä yhteydessä Knowledge.co.id: n ympärillä keskustelemme siitä, mitä paine on ja mitä muita elementtejä ovat peitti sen. Katsotaan…
- Dynaamiset nesteet: tyypit, ominaisuudet, Bernoullin yhtälö, lauseet… Dynaamiset nesteet: tyypit, ominaisuudet, Bernoullin yhtälö, Toricellin lause, kaavat ja esimerkkejä ongelmista - mikä se on dynaamiset nesteet ja niiden tyypit? noin…
- Veden tiheys: määritelmä, kaavat ja esimerkit Veden tiheys: määritelmä, kaavat ja esimerkit - Mikä on veden tiheys? Katsotaan yhdessä…
- Määrän, yksikön, mittauksen ja esimerkit… Määrän, yksikön, mittauksen ja esimerkit (täydellinen) - Fysiikan peruskäsitteissä olemme varmasti tutustuneet johonkin jokapäiväiseen elämään liittyvään. Kuten korkeuden, punnitusmassan, leveyden mittaaminen...
- Esimerkkejä tieteellisestä työstä: Kielen funktiot ja säännöt Esimerkkejä tieteellisistä kirjoituksista: funktiot ja kielen säännöt - Mitkä ovat esimerkkejä hyvistä ja oikeista tieteellisten julkaisujen kirjoittamisen muodoista? Aiemmin Seputar the Knowledge.co.id on käsitellyt tieteellistä työtä: määritelmää, ominaisuuksia, etuja,…
- Esimerkkejä litteistä muodoista: litteiden muotojen tyypit, ominaisuudet ja kaavat Esimerkkejä litteistä muodoista: litteiden muotojen tyypit, ominaisuudet ja kaavat – mitkä ovat esimerkkejä litteistä muodoista?
- Esimerkki fyysisen kasvatuksen kysymyksistä luokan 11 (XI) SMA/MA/SMK lukukauden 1 ja 2 Esimerkkejä liikuntakysymyksistä luokan 11 (XI) SMA/MA/SMK lukukauden 1 ja 2 (2019 ja 2020) aikana – Seputarknowledge.co.id käsittelee esimerkkejä luokan 11 monivalintakysymyksistä ja esseistä. ...
- Sademäärä on: 12 määritelmää asiantuntijoiden, tyyppien,… Sademäärä on: 12 määritelmää asiantuntijoiden tyyppien ja tekijöiden mukaan - Tässä keskustelussa Around Knowledge selittää sateesta. Sade on ilmastollinen ilmiö, joka on luonnollinen...
- √ Kemiallisten yhdisteiden määritelmä, ominaisuudet, tyypit ja nimikkeistö… Kemiallisten yhdisteiden määritelmä, ominaisuudet, tyypit, täydellinen nimikkeistö - Tässä keskustelussa selitämme kemiallisia yhdisteitä. Kattaa kemiallisten yhdisteiden määritelmän, ominaisuudet, tyypit ja nimikkeistön keskustelun kanssa...
- Yksittäiset aineet ovat: määritelmä, alkuaineet ja yhdisteet Yksittäiset aineet ovat: määritelmät, elementit ja yhdisteet – mitä yksittäinen aine tarkoittaa? Katsotaanpa keskustelua yhdessä...
- Kalteva taso: määritelmä, kaavat, mekaaninen etu ja… Vino taso: määritelmä, kaavat, mekaaniset edut ja esimerkkejä ongelmista - mitä tasolla tarkoitetaan vino ja miten lasketaan fysiikka? luonnollisesti…
- Yksikkömuunnos: määritelmä, kerroin, pituus, massa, aika,… Yksikkömuunnos: määritelmä, kerroin, pituus, massa, aika, tilavuus ja paine - mikä on yksikkömuunnos?, Tällä kertaa Seputarknowledge.co.id keskustelee siitä, mukaan lukien tekijät, tyypit ja tietysti muut asiat Mikä…
