Kolloidse aine kokkuvõte: omadused, tüübid, näited
Laadimine...
Tere poisid! Kas teadsite, et üks näide kolloidist on või, toit, mida sageli koos leivaga tarbitakse. Aga tuleb välja, et neid on ikka palju sa tead veel üks näide kolloididest, mida me sageli igapäevaselt leiame.
Mis need on? Vastuse leidmiseks lugege see artikkel hoolikalt läbi!
Sisu loetelu
Kolloidi määratlus

Kolloidid on teatud tüüpi heterogeensed segud, mis moodustuvad aine hajumisel teiste segatud ainetega. Seetõttu on kolloidsüsteemis dispersioonikeskkond ja dispergeeritud faas.
Dispergeeriv keskkond on aine, mis põhjustab ühtlase jaotumise. Samal ajal on hajutatud faas aine, mis jaotub teistes ainetes ühtlaselt.
Näiteks kookospiimas nimetatakse kookospiimas sisalduvaid graanuleid dispergeeritud faasiks, vett aga dispergeerivaks keskkonnaks.
Teised kolloidsüsteemide näited on värv, juust, majonees, tarretis, veri ja palju muud. Niisiis, meie igapäevaelu on tihedalt seotud kolloidsüsteemiga.3
Loe: Molaarsuse valem
Kolloidsed omadused
1. Tyndalli efekt

Kolloidide olemuse avastas esmakordselt Inglismaa füüsik John Tyndall. Tyndalli efekt on valguse hajumine kolloidosakeste poolt. Kui valguskiir on suunatud lahusesse, kandub valgus edasi.
Selle tulemusena me ei näe valgust. Selle põhjuseks on lahuse homogeensus ja kolloidmolekuli suur suurus.
2. Browni liikumine

Browni liikumine on kolloidosakeste liikumine, mis on sirge, kuid ebakorrapärases või juhuslikus suunas. Ultramikroskoobiga vaadates näeme kolloidosakesi, mis liiguvad siksakidena. Seda siksak-liikumist nimetatakse Browni liikumiseks, mis toimub ainult vedelikes ja gaasides.
Seda seetõttu, et vedeliku või gaasi kolloidosakeste liikumine põhjustab kolloidosakeste endi kokkupõrkeid. Kokkupõrge toimus igast suunast ja selle tulemuseks oli tasakaalutus, mis põhjustas siksakilise liikumise.
Mida väiksem on osakeste suurus, seda kiiremini toimub Browni liikumine. Teisest küljest, mida suurem on osakeste suurus, seda aeglasem on Browni liikumine.
See selgitab, miks Browni liikumist ei ole lahuses lihtne jälgida ega leiduda ka heterogeensetes tahkete ainete segudes vedelike või suspensioonidega.
3. Adsorptsioon

Adsorptsioon on osakeste, ioonide või muude ühendite adsorptsiooniprotsess kolloidosakeste pinnal osakeste suure pindala tõttu.
4. Kolloidne koagulatsioon
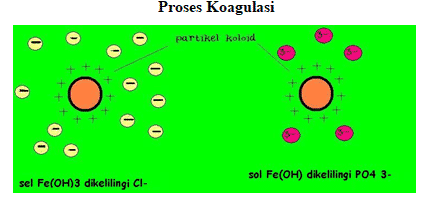
Kolloidne koagulatsioon on kolloidosakeste kokkukleepumine ja sademe moodustumine. Selle tulemusena ei moodusta hajutatud aine enam kolloidi. Need sündmused võivad kergesti tekkida füüsiliselt, nagu jahutamine ja segamine, ja keemiliselt, näiteks elektrolüütide lisamisel.
5. Kaitsev kolloid
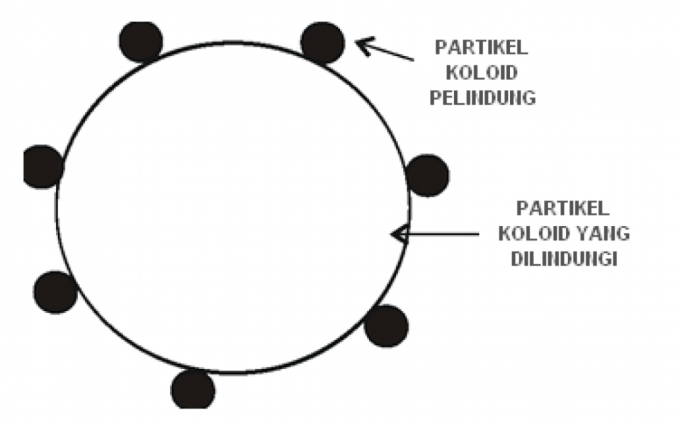
Kaitsekolloidid on kolloidsed omadused, mis võivad kaitsta teisi kolloide hüübimisprotsesside eest.
6. Dialüüs

Dialüüs on protsess, mille käigus eraldatakse kolloidid segavatest ioonidest kolloididega segatud vedeliku voolamise teel läbi poolläbilaskva membraani filtrina. Seda poolläbilaskvat membraani võib vedelik läbida, kuid kolloid ei pääse läbi.
7. Elektroforees
Reklaam

Kolloidide viimane omadus on elektroforees ehk laetud kolloidosakeste eraldamine elektrivoolu abil.
Kolloidide tüübid

Kolloidid jagunevad 8 (kaheksa) tüüpi, millel on järgmised üksikasjad:
1. Tugev tald
Tahke sool koosneb tahkest dispergeeritud faasist ja tahkest dispergeerivast keskkonnast. Tahke sooli moodustumist mõjutavad rõhk ja temperatuur, nii et moodustub tahke ja kõva tahke aine. Tahke sooli näide on vääriskivi (rubiin).
2. Sol
Sool koosneb tahkest dispergeeritud faasist ja vedelast dispersioonikeskkonnast, mistõttu selle omadusi ei ole lihtne muuta. Sooli ja tahke sooli erinevus seisneb dispersioonikeskkonnas.
3. Tahke aerosool
Tahketel aerosoolidel on gaasilises dispersioonikeskkonnas tahke dispergeeritud faas. Tahke aerosooli näide on sõiduki aurud. Seetõttu tunneme mõnikord sõiduki aurudega kokku puutudes virvendust, kuna sõiduki suitsul on tahkete ainete kujul hajutatud faas.
4. Aerosool
Aerosool on teatud tüüpi kolloid, millel on hajutatud faas vedeliku kujul ja dispersioonikeskkond gaasi kujul. Aerosoolid ei kesta kaua, sest nende koostisained saavad õhurõhu ja keskkonnatemperatuuri muutuste tõttu kergesti kahjustada.
5. Tahke emulsioon
Tahke emulsioon koosneb vedelast dispergeeritud faasist ja tahkest dispersioonikeskkonnast. Näiteks želatiin, kus dispergeeritud faasiks on vesi ja dispersioonikeskkonnaks pulber.
6. Emulsioon
Emulsioon on teatud tüüpi kolloid, milles dispergeeritud faas ja dispersioonikeskkond on vedelad. Tavaliselt koosnevad emulsioonid erineva polaarsusega ühenditega vedelikest. Seega ei segune vedelikud omavahel.
7. Tahke vaht
Tahkel vahul on gaasiline dispergeeritud faas ja tahke dispersioonikeskkond. Tahket vahtu võib nimetada ka tahkes dispergeeritud gaasiks.
8. vahutama
Vahul on gaasiline dispergeeritud faas ja vedel dispersioonikeskkond. Vaht on tuntud ka kui vedelikus dispergeeritud gaas.
Loe: Iooniline side
Kolloidi näidete tabel

| Ei. | Hajutatud faas | Dispersioonikeskkond | Tüüp | Näide |
| 1. | Gaas | Vedelik | vahutama | Vahukoor, seebivaht |
| 2. | Gaas | Ülekoormatud | Tahke vaht | Pimss, vahtkumm |
| 3. | Vedelik | Gaas | Aerosool | Udu |
| 4. | Vedelik | Vedelik | Emulsioon | Kookospiim, piim, kalaõli |
| 5. | Vedelik | Ülekoormatud | Tahke emulsioon | Tarretis, opaal, pärl |
| 6. | Ülekoormatud | Gaas | Aerosool | Tolm õhus |
| 7. | Ülekoormatud | Vedelik | Sol | Värv, tint, kuldne tald |
| 8. | Ülekoormatud | Ülekoormatud | Tugev tald | Must teemant, värviline klaas |
Kolloidne valmistamine

Kui varem oleme arutanud kolloidide tüüpide tähendust. Niisiis, kuidas teha kolloide? Kolloidide valmistamine on järgmine:
1. Kuidas kondenseerida
Kolloidide valmistamine kondensatsiooni teel on lahuseosakeste või väikeste osakeste kombineerimine suuremate osakestega. Lühidalt öeldes ühendab see meetod olemasolevad kolloidid väiksemate osakestega.
2. Hajutamise viis
Dispersioon on suurte osakeste (suspensioon) purustamine väikesteks osakesteks (kolloidideks). Sellel meetodil on kolm etappi, nimelt peptimine, aretuskaar ja mehaanika.
Loe: Kvantmehaanika
Kolloidide eelised

1. Valgendav suhkur
Suhkrut, mille värvus on endiselt tuhm, pleegitatakse tavaliselt kolloidide abil. Nipp seisneb selles, et suhkur lahustatakse vees, seejärel lastakse lahus läbi kolloidse kobediatomiitmulda süsteemi.
2. Saasteainete vähendamine õhus
Võrefiltr on seade, mida kasutatakse suitsu ja kahjulike osakeste absorbeerimiseks tehase heitgaasidest. Selle tööriista töös rakendatakse kolloidse aglomeratsiooni põhimõtet ja laengu olemust, nii et eralduv õhk on vaba kahjulikest saasteainetest.
3. Neerupuudulikkusega patsientide dialüüsiprotsessi abistamine
Dialüsaatorid või dialüüsiprotsessis (dialüüsis) kasutatavad seadmed eraldavad kolloidosakesi ja nende lahustunud aineid.
Näited kolloidsüsteemi probleemidest

Kolloidide omadust, mida nimetatakse võimeks valgust hajutada, nimetatakse...
- Tyndalli efekt
- Dialüüs
- Browni liikumine
- Adsorptsioon
- Elektroforees
Vastus: A
Majonees on teatud tüüpi kolloid...
- vahutama
- Aerosool
- Sol
- Emulsioon
- Tahke vaht
Vastus: A
Vahukoor on kolloidne süsteem, milles dispergeeritud faas ja dispersioonikeskkond koosnevad…
- Vedel ja tahke
- Tahke ja gaasiline
- Tahke ja vedel
- Gaasiline ja tahke
- Gaas ja vedelik
Vastus: E
Noh, see on kõik arutelu ja näited kolloidide kohta. Lõpuks tuleb märkida, et kolloidid on keemiaainetes üks olulisi materjale. Head õppimist!
X SULGE
Reklaamid
REKLAAM
X SULGE
