Ühendite, liikide, kirjutamise reeglite ja näidete mõistmine (täielik)
Ühendite, liikide, kirjutamise reeglite ja näidete mõistmine (täielik) - Selles arutluses selgitame ühendite kohta. Mis hõlmab ühendite mõistmist, ühendite tüüpe, ühendite kirjutamise reegleid ja ühendite näiteid, mida arutatakse täielikult ja kergelt. Lisateabe saamiseks lugege palun hoolikalt allolevaid ülevaateid.
Sisukord
-
Ühendite, liikide, kirjutamise reeglite ja näidete mõistmine (täielik)
- Ühendi määratlus
-
Keemiliste valemite ja lihtsate liitnimede kirjutamise reeglid
- 1. Metallist ja mittemetallist ühendid
- 2. Mittemetall ja mittemetallühend
- Näited ühenditest elus
- Jaga seda:
- Seonduvad postitused:
Ühendite, liikide, kirjutamise reeglite ja näidete mõistmine (täielik)
Arutleme kõigepealt hoolikalt ühendite tähendust.
Ühendi määratlus
Ühend on aine, mis koosneb kahest või enamast erinevast elemendist ja mida saab keemilise reaktsiooni abil jagada lihtsamateks aineteks.
Näitena võib tuua toiduvalmistamisel loomulikult sageli vett, soola, suhkrut ja muid lõhna- ja maitseaineid. Need ained on ühendi näide. Vesi koosneb vesiniku ja hapniku elementidest, sool koosneb naatriumi ja kloori elementidest, suhkur koosneb süsiniku, vesiniku ja hapniku elementidest.
Neid ühendeid kohtab sageli igapäevaelus. Ja muidugi oleme sellega harjunud. Aga kuidas protsess ja nimetamine, siis järgige selgitust.
Soola saab keemiliste reaktsioonide abil jagada naatriumiks ja klooriks. Ühendi väikseimat osa võib nimetada molekuliks. Suurtes kogustes ühendatud molekulid moodustavad ühendi. Nagu veeühend, mis koosneb miljonitest veemolekulidest.
Keemiliste valemite ja lihtsate liitnimede kirjutamise reeglid
Lihtne ühend on aine, mis koosneb kahest erinevast elemendist. Lihtsate ühendite näideteks on vesi (H2O), sool (NaCl), metaan (CH4), vääveldioksiid (SO2) ja nii edasi. Nüüd vaadake allolevat tabelit hoolikalt: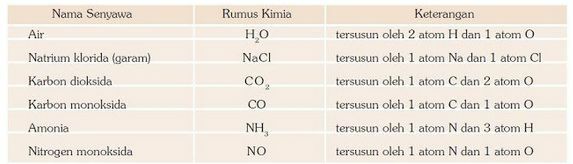
Loe ka:Alternatiivenergia: mõistmine ekspertide, omaduste, eeliste, tingimuste ja tüüpide järgi
Lihtne ühend võib koosneda metallist elementidest ja mittemetallidest või mittemetallidest mittemetallidest. Ühendite nimetamise reeglid põhinevad neid moodustavate elementide tüübil.
Seetõttu on ühendite nimetamise reeglid jagatud kaheks osaks, nimelt reeglid lihtsa ühendi nime kirjutamiseks, mis koosneb metallist ja mittemetallist elementidest ning ka mittemetalsetest elementidest koosneva lihtsa ühendi nime kirjutamise reeglid ja mittemetall.
1. Metallist ja mittemetallist ühendid
Metallist ja mittemetallist elementidest koosneva lihtsa ühendi nime kirjutamise reeglid on järgmised:
- Kõigepealt kirjutatakse metallelemendi nimi
- Mittemetalliliste elementide nimed kirjutatakse metallelementide nimede järele ja lisatakse järelliitega -ide
Näide:
- NaCl koosneb naatriumist (metall) ja kloorist (mittemetall), seega on NaCl nimi: naatrium (metall) + kloriid (mittemetall)
- MgCl2 koosneb magneesiumist (metall) ja kloorist (mittemetall). Niisiis on MgCl2 nimi: magneesium (metall) + kloriid (mittemetall).
2. Mittemetall ja mittemetallühend
Mittemetallist elemendist koosnevate lihtsate elementide nimede kirjutamise reeglid on järgmised:
- Kõigepealt kirjutatakse esimese mittemetallilise elemendi nimi
- Teise mittemetallilise elemendi nimi kirjutatakse esimese mittemetalli järele, alustades elemendi aatomnumbrist ladina keeles ja lõpetades järelliitega -ide.
- Kui esimese mittemetallilise elemendi aatomite arv on rohkem kui üks, algab kirjutamine elemendi aatomite arvuga ladina keeles.
Ladina keeles elementide aatomite arvu leiate allolevast tabelist: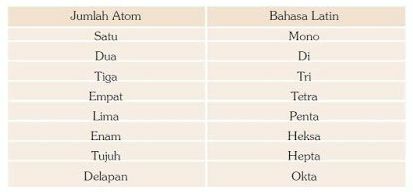
Näide:
- CO2 koosneb 1 süsinikuaatomist (mittemetallist) ja 2 hapnikuaatomist (mittemetallist), seega on CO2 nimetus süsinikdioksiid.
- N2O4 koosneb 2 lämmastikuaatomist (mittemetallid) ja 4 hapnikuaatomist (mittemetallid), seega on N2O4 nimi dinitrogeentetraoksiid.
Loe ka:Kaldus tasand: määratlus, valem, mehaaniline eelis ja näiteülesanded
Näited ühenditest elus
Ühendeid võib saada otse loodusest või toota inimene keemilise protsessi abil. Looduses esinevad ühendid tekivad keemiliste protsesside kaudu, mis toimuvad looduslikult, näiteks vulkaanilises tegevuses, mis tekitab gaasi SO2.
Otse loodusest saadud ühendid on mineraalidena, näiteks vesi, sool merevees, lubjakivi, gaas SO2, gaasiline süsinikdioksiid. Inimeste toodetud ühendite hulka kuuluvad suhkur, alkohol, seep, lõhna- ja maitseained ning mitmesugused muud tüüpi valgud.
Seega on selle kohta selgitatud Ühendite, liikide, kirjutamise reeglite ja näidete mõistmine (täielik)loodetavasti saab teie ülevaadet ja teadmisi täiendada. Täname külastamast ja ärge unustage teisi artikleid lugeda.
