Prootoni määratlus, struktuur, omadused, laeng, ajalugu ja näited
Prootoni määratlus
Prootonid on subatoomiliste osakeste tüüp, mis on üks minimaalsetest aatomi moodustavatest osakestest. See prooton kuulub fermionide perekonda ja on varustatud ka positiivse elektrilaenguga.
Kogu aine koosneb aatomitest ja see omakorda koosneb 3 tüüpi osakestest, mis on varustatud erinevate elektrilaengutega:
- elektronid (negatiivne laeng),
- neutronid (neutraalne laeng) ja
- prootonid (positiivne laeng).
Pikka aega arvati, et prooton on põhiline osakeste tüüp, see tähendab, et see on jagamatu või jagatav. Kuid täna on kindlaid tõendeid selle kohta, et need prootonid koosnevad kvarkidest.
See prooton on aga stabiilne subatoomne osake, elektroniekvivalent. Erinevalt elektronidest, mis tiirlevad ümber aatomituuma, asuvad need prootonid aatomituumas neutronite kõrval, mis annavad suurema osa aatomi massist.
Prootoni avastamise ajalugu

Ernest Rutherford avastas prootoni lämmastikuga katsetades. Prootoni avastas 1918. aastal Ernest Rutherford (1871–1937), inglise keemik ja füüsik. Lämmastikgaasiga tehtud katsete keskel märkis Rutherford hiljem, et tema seade tuvastas vesiniku tuumade olemasolu, tulistades gaasi alfaosakesi.
Ta jõudis järeldusele, et tuum peab olema aine põhiosake, teadmata tol ajal, et täpsemalt öeldes sisaldab vesiniku aatomi tuum ühte osakest: prootonit. Seega otsustati vesinik varustada aatomnumbriga 1.
Siiski oli teada ka varasem teaduslik kogemus, mis selle avastamiseni viis. üks näide, saksa füüsik Eugene Goldstein (1850–1930) aastal 1886 järeldusele, et aatom muutus elektriliselt neutraalseks.
Peale selle, J. J. Thompson (1856–1940) Inglismaalt pärit on või on avastanud negatiivse laenguga elektrone, see tähendab, et aatomis peab olema mingisugune vastupidise laenguga osake. Kuid nende osakeste otsimisel leidis Goldstein katoodkiirtega katsetades hiljem positiivseid ioone.
Prootonite omadused ja omadused
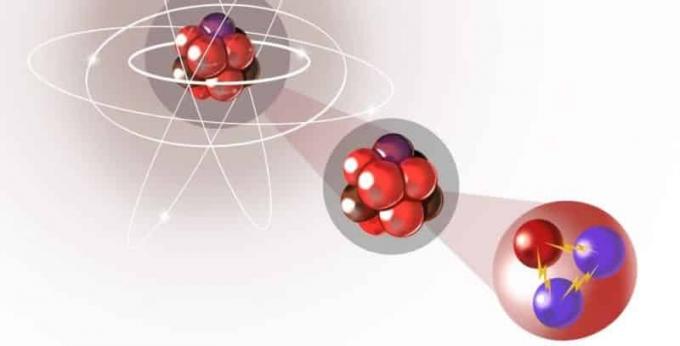
Kõik need prootonid koosnevad kahest "üles" ja 1 "allapoole" kvarkist.
Prooton on stabiilne liitosake, palju suurem kui elektron (1836 korda) ja millel on ka positiivne elementaarlaeng 1 (1,6 x 10 ^ -19 C). Prootonid ise koosnevad kolmest elementaarosakesest või kvarkist: kahest "üles" (üles) ja ühest "alla" (alla). Nende poolestusaeg on pikem kui 1035 aastat, mis on siis, kui nad on vastuvõtlikud lagunemisele.
Sellel prootonil, nagu teistelgi subatomaarsetel osakestel, on oma spinn, nimelt sisemine ja muutumatu nurk, mis antud juhul on. See omadus on väga kasulik nii tuumamagnetresonantsi kui ka teiste kaasaegsete tehnoloogiliste rakenduste jaoks.
Prootoni struktuur
Nendel prootonitel ja neutronitel on ka struktuur. Prootonite ja neutronite seest leiame tõelisi elementaarosakesi, mida nimetatakse kvarkideks. Tuuma sees seovad prootonid ja neutronid omavahel võimsate jõududega, põhiliste vastasmõjudega, mis reguleerivad üksikute prootonite ja neutronite moodustavate kvarkide käitumist.
Prootonil on uudsete kvarkide koostis, seega on laengu kvantarv:
q (uud) = + + (-1/3) = +1
Selle prootoni mass on 938 272 MeV / c2, samas kui nende kolme kvarki mass on ainult umbes 12 MeV / c2 (ainult umbes 1% neutroni massienergiast). Nagu prootonid, on ka suurem osa nende neutronite massist (energiast) tugeva tuumajõu (gluuonide) energia kujul. Neutronkvarke hoiavad koos gluunid, mis vahetavad osakesi tugeva tuumajõu vastu.
Prootoni stabiilsus

Need vabad prootonid (prootonid, mis ei ole seotud nukleonide ega elektronidega) on stabiilsed osakesed, mille puhul pole täheldatud spontaanset lagunemist teisteks osakesteks. Neid vabu prootoneid leidub loomulikult paljudes olukordades (nt nad moodustavad 90% kosmilised kiired), milles energia või temperatuur on piisavalt kõrge, et eraldada neid elektronidest, millel on afiinsus.
Prootonite lagunemist seostatakse ka barüoni arvu säilimise seadusega. Baryoni arv on nukleoni arvu üldistus, mis on säilinud mitterelativistlikes reaktsioonides ja tuuma lagunemises. Baryoni arvude säilimise seadus ütleb, et:
Kõigi sisenevate osakeste barüoniarvude summa on sama, mis kõigi reaktsioonist tulenevate osakeste barüoniarvude summa.
aatomituum

Kuna neid leidub tavaliselt aatomi tuumas, on prootonid ja neutronid tuntud kui "nukleonid". Elektroonid seevastu tiirlevad nende ümber enam-vähem levik.
Need aatomituumad on omavahel ühendatud tugeva tuumajõuga, mis on ainult suurte aatomite (näiteks Uraan) puhul, mis võivad või võivad tekitada muid jõude, näiteks elektromagnetikat.
Need nukleonid moodustavad mis tahes aatomi suurima massiprotsendi ja määratlevad seetõttu erinevuse keemiliste elementide ja teiste vahel: näiteks selle vesiniku aatomi tuumas on ainult üks prooton, heeliumis aga 2 prootonit ja üks või kaks neutronit, sõltuvalt isotoopist Konkreetsed.
aatomnumber
Iga elemendi aatomnumbrit saab või näeb perioodilisustabelis.
Aatomnumber (Z) näitab, kui palju prootoneid on teatud tüüpi aatomitel oma tuumas. igal keemilisel elemendil on erinev aatomnumber, kuigi selle keemilise käitumise määrab mõnevõrra tuuma ümber tiirlevate elektronide arv.
Nii on näiteks kloori (Cl) tuumas 17 prootonit, seega on selle aatomnumber 17. See arv ei erine kunagi, isegi sama aatomi isotoopide (versioonide) vahel, sest need erinevad üksteisest ainult nende tuumade neutronite arvu poolest.
Prootoni laadimine ja missa
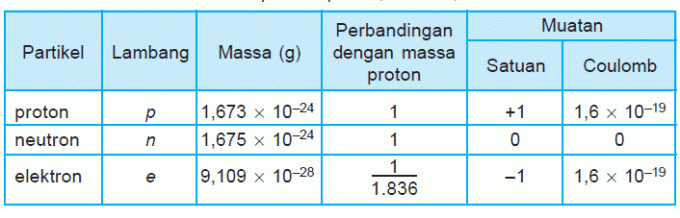
Füüsikas on see prooton subatoomiline osake, mille positiivne laeng on 1,6 × 10-19 kulonbi ja mass 938 MeV (1,6726231 × 10-27 kg ehk umbes 1836 korda suurem kui elektron). Aatom koosneb tavaliselt paljudest prootonitest ja neutronitest, mis paiknevad aatomi tuumas (keskel), samuti mitmest tuuma ümbritsevast elektronist. Neutraalselt laetud aatomi korral on prootonite arv võrdne elektronide arvuga. Prootonite arv tuumas määrab tavaliselt aatomi keemilised omadused. Seda aatomituumat tuntakse sageli tuuma, tuuma või ka tuumana (inglise keeles nucleon) ning nende aatomituumadega toimuvaid või seotud reaktsioone nimetatakse tuumareaktsioonideks.
Füüsikalised omadused
Nende prootonite mass on veidi väiksem kui tuumas olevate neutronite massil, kuid need on 1836 korda suuremad kui elektronid. Prootoni tegelik mass on 1,6726 x 10 ^ -27 kilogrammi, mis on väga väike mass. Sümbol “^ -” tähistab negatiivset eksponenti. See number on kümnendkoht, millele järgneb 26 nulli, seega number 16726. Elektrilaengu osas on prootonid positiivsed. Mitte elementaarosakestena on prootonid tegelikult valmistatud 3 väikesest osakesest, mida nimetatakse kvarkideks.
Funktsioonid Atomis
Aatomi tuumas olevad prootonid aitavad tuuma omavahel siduda. Need prootonid meelitavad ka negatiivselt laetud elektrone ja hoiavad neid tuuma ümber orbiitidel. Selle aatomi tuumas olev prootonite arv määrab, milline keemiline element see on. Seda arvu nimetatakse aatomnumbriks; tähistatakse sageli suurtähega "Z".
Eksperimentaalne kasutamine
Massiivse osakeste kiirendi sees kiirendavad need füüsikud prootoneid väga suurele kiirusele ja sunnivad neid ka kokku põrkama. See loob teise osakeste kaskaadi, mida füüsikud on sellest ajast alates uurinud. Šveitsi CERN-i osakeste füüsikalabor põrkab kokku prootonitega, et nende siseruumide struktuuri uurida, kasutades kiirendajat nimega Large Hadron Collider (LHC). Seejärel piiravad neid osakesi tugevad magnetid, mis hoiavad neid enne kokkupõrget selles 27-kilomeetrises ringis liikumas.
Katse sarnaneb eesmärgiga luua väikeses mahus mateeria vormid, mis eksisteerisid millalgi pärast Suurt Pauku.
Energia tähtede jaoks
Päikeses ja kõigis teistes tähtedes kombineeruvad need prootonid teiste prootonitega tuumasünteesi abil. See termotuumasüntees vajab siis umbes 1 miljon kraadi Celsiuse temperatuuri. Kõrge temperatuur põhjustab 2 kergema osakese sulamist kolmandaks osakeseks. Loodud osakese mass on väiksem kui kaks algset osakest kokku.
Seejärel avastas Albert Einstein 1905. aastal, et ainet ja energiat saab või saab muuta ühest vormist teise. See seletab, kuidas termotuumasünteesi käigus kaotatud massikadu ilmub tähe eraldatava energiana.
Prootoni näide
Vabad prootonid on olemas. Vesiniku aatomi tuum või ka H + ioon on prootoni näide. Isotoopist olenemata on igal vesiniku aatomil 1 prooton; iga heeliumi aatom sisaldab 2 prootonit; iga liitiumiaatom sisaldab 3 prootonit ja nii edasi.
Seega võib prootoni definitsiooni, struktuuri, omaduste, laengu, ajaloo ja näidete selgitus loodetavasti teile kasulik olla. Aitäh
Vaata kaOskuste, liikide, näidete ja ekspertide mõistmine
Vaata kaBullet Rejecti, tehnika, välja, reeglite ja stiili määratlus
Vaata kaMaksud: määratlus, funktsioonid, eelised ja tüübid ekspertide sõnul
