Ensüümid on: määratlus, kuidas see toimib, funktsioonid, omadused (täielik)
Haridus. Co ID Ensüümid on tihedalt seotud igasuguste ainevahetusprotsessidega, mis organismi kehas esinevad. Ainevahetus ei ole täielik ilma ensüümideta, mis on siis ensüümid? Ja kuidas see toimib ja selle roll ainevahetusprotsessis? Siin on täielik kirjeldus.
Ensüümide määratlus
Ensüüm on valguühend, mis koosneb valgu komponentidest ja on ka katalüütiline, mille ülesanne on organismi ainevahetusprotsessi kiirendamine. Miks on see komponent ainevahetusprotsessis nii oluline, sest see suudab kiirendada, vähendades metaboolsete reaktsioonide alustamiseks vajalikku aktiveerimisenergiat.
Sõna ensüüm pärineb kreekakeelsest sõnast, mis tähendab pärmi. Louis Pasteuri poolt läbi viidud alkohoolse kääritamise katse sai verstapostiks seoses ensüümide avastamisega. Ensüümid on ühendid, mis koosnevad valkudest (apoensüümid) ja mittevalgulistest ühenditest (kofaktorid).
Katalüütilised omadused on ensüümide omadused, mis eristavad ensüüme teistest valkudest. Katalüütilised omadused saadakse kofaktorirühmadelt, milleks võivad olla orgaanilised ühendid (koensüümid ja proteesirühmad) või anorgaanilised ühendid (metalliioonid).
Kuidas ensüümid töötavad
Ensüümide toimimine organismi metaboolses reaktsioonis on: alandades aktivatsioonienergiat, mis on reaktsiooni käivitamiseks vajalik energia. "Kulude" minimeerimisel on ka toimuv protsess kiirem. Keemilise reaktsiooni aktivatsioonienergiat saab võrrelda "teekuludega" tootmisprotsessis. Mida madalamad on jooksvad kulud, seda kiirem on protsess.
Lisaks sellele on ensüümide kasutamise eelis see, et lisaks "odavamale" toimimisele on reaktsiooniprotsess stabiilne toimub nii nagu peab, sest see ainevahetusprotsessi soodustav ensüüm ei osale reageerima.
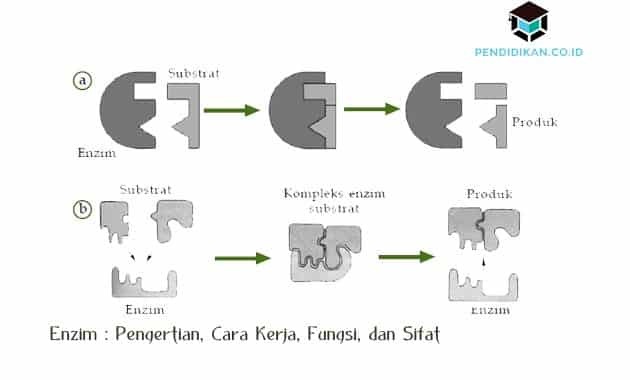
Ensüümide töö keemiliste reaktsioonide kiirendamisel on substraadiga suhtlemine, mille järel substraat muudetakse tooteks. Toote moodustumisel vabaneb ensüüm substraadist. Seda seetõttu, et ensüüm ei reageeri substraadiga. Ensüümide toimimist kirjeldavad kaks teooriat, sealhulgas järgmine:
Lukusta ja lukusta teooria
Selle teooria avastas 1894. aastal Emil Fischer. Tema sõnul seondub ensüüm substraadiga, millel on sama kuju (konkreetselt) kui ensüümi aktiivsel saidil. Teisisõnu saavad ensüümiga suhelda ainult konkreetselt sobiva kujuga substraadid.
Sellepärast nimetatakse seda luku ja võtme teooriaks, kus ensüümi illustreeritakse lukuna ja substraati nimetatakse lukuks. sest tabalukul ja võtmel on sama külgkinnitus, et neid saaks avada või vastupidi.
Sellel teoorial on puudus, mis ei suuda seletada ensüümi stabiilsust ensüümi reaktsioonipunkti ülemineku ajal. Teine teooria on induktsiooni teooria.
Induktsiooniteooria
Selle teooria pooldaja oli Daniel Koshland 1958. aastal, ensüümidel on paindlik aktiivne koht. Ent ensüümi aktiivsel saidil on samad seondumispunktid / spetsiifilised. Nii et ainult substraat, millel on samad spetsiifilised sidumispunktid, indutseerib ensüümi aktiivse koha nii, et see sobiks (moodustub nagu substraat).
Induktsiooniteooria Induktsioon suudab vastata eelmise luku ja võtme teooria puudustele. Seetõttu on Daniel Koshlandi poolt 1958. aastal välja pakutud induktsiooniteooria teadlaste poolt enim tunnustatud teooria ensüümide toimimise selgitamiseks.
Ensüümi funktsioon
- Ensüümidel on keemilises reaktsioonis väga oluline roll. Nagu selgitatud, on ensüümide ülesanne keemilise reaktsiooni kiirendamine organismi kehas. Ensüümideta on häiritud nii anabolismi kui ka katabolismi ainevahetusprotsessid.
- Peale selle on ensüümi olemus, mis substraadiga ei reageeri, kõige kasulikum keemiliste reaktsioonide kiirendamiseks organismi kehas.
Ensüümi omadused
Ensüümide roll on organismide ellujäämisel väga oluline. Seetõttu peame teadma, millised on selle ensüümi omadused. Allpool on ensüümide omaduste kirjeldus, mida peame teadma:
Biokatalüsaator
on biokatalüsaator, mis tähendab, et ensüüm on katalüsaatorühend, mis on ühend, mis kiirendab keemilist reaktsiooni reageerimata. Kuna need ensüümid pärinevad organismidest, nimetatakse neid ka biokatalüsaatorite ühenditeks.
Termolabiil
Osa ensüümi struktuurist on valguühend. Seetõttu on ensüümidel ka termolabiilsed omadused, see tähendab, et temperatuur mõjutab neid ensüüme tugevalt. Ensüümidel on optimaalne temperatuur oma funktsioonide täitmiseks. Üldiselt töötavad ensüümid optimaalselt temperatuuril 37ºC. Kui äärmuslikel temperatuuridel võib kahjustada ensüümide tööd. Ensüüm on mitteaktiivne temperatuuril alla 10 ° C, samas kui see denatureeritakse temperatuuril üle 60 ° C. Seetõttu on jahutamisprotsess üks toidu säilitamise protsessidest, kuna riknenud bakterite ensüümid ei suuda toitu seedida.
Samal ajal võib kuumutamise või kõrgel temperatuuril põletamise protsess kahjustada ensüümi struktuuri või ensüüm kogeb denaturatsiooni. On mõned erandid, näiteks iidsetes bakterirühmades, mis elavad väga äärmuslikes piirkondades, näiteks metanogeenid, mille elukeskkonnas on kõrge temperatuur, on neil ensüümid, mis töötavad optimaalselt madalamal temperatuuril 80 C.
Konkreetsed
Nagu on kirjeldatud kahes ensüümide toimimise teoorias, on need ensüümid spetsiifilised, mis tähendab, et siin seondub ensüüm substraadiga, mis on võimeline seonduma ensüümi aktiivse saidiga. Substraadil on sama seondumispunkt, mis põhjustab substraadi seondumise ensüümiga. Nimetamise aluseks on ka ensüümi spetsiifiline olemus. Selle ensüümi nimi võetakse tavaliselt ka seotud substraadi tüübist või toimuva reaktsiooni tüübist. Näiteks on amülaas ensüüm, mis mängib rolli tärklise, mis on polüsahhariid (komplekssuhkur), lagundamisel lihtsamateks suhkruteks.
Mõjutatud pH-ga
Nii nagu temperatuur, mõjutab pH või happesuse aste ka ensüümide tööd. Põhimõtteliselt töötab ensüüm neutraalses atmosfääris (6,5–7). Mõni ensüüm on optimaalne happelise pH juures nagu pepsinogeen või leeliselise pH juures nagu trüpsiin.
Töötage edasi-tagasi
Ensüümid, mis lõhustavad ühendi A B-ks, samuti ensüümid, mis aitavad moodustada ühendist B ühendist A. Sellepärast nimetatakse ensüümi vastupidiseks toimimiseks.
Ei määra reaktsiooni suunda
Ühendi A muutumine B-ks või vastupidine ei ole ensüüm, mis määrab reaktsiooni kulgemise suuna. Vajalikumad ühendid on punktid keemilise reaktsiooni suunast. Näiteks kui kehal puudub glükoos, suudab ta lagundada varusuhkrut (glükogeeni) ja vastupidi.
Mõned ensüümide kirjeldused: mõistmine, töömeetodid, funktsioonid ja omadused, loodetavasti võib see teile kasulik olla.
Vaata kaSotsiaalse kontrolli määratlus, tüübid, funktsioonid, meetodid ja vormid
Vaata kaAnoomia, kultuurilanguse, Mestizo kultuuri mõistmine ja näited
Vaata kaAnabolismi mõiste
