HEAT: Formeln, Typen, Beispielaufgaben (Zusammenfassung)
Wird geladen...
Die Wärmeformel ist aus dem Physikunterricht bekannt. Wärme ist eine Energieform, die von einem Objekt aufgenommen oder abgegeben werden kann. Wärme hat Einheiten, die Joule oder Kalorien genannt werden.
Wärme kann als Wärmeenergie interpretiert werden, die bestimmte Substanzen besitzen, und kann durch Messen der Temperatur des Objekts nachgewiesen werden. Sie können die Anwendung von Wärme auf warmes Wasser sehen, das offen gelassen wird und allmählich abkühlt (nicht mehr warm wird), weil Wärme aus dem Wasser an die Luft abgegeben wird.
Inhaltsverzeichnis
Definition von Kalorien

Wärme ist eine Energie, die sich von einem Objekt mit höherer Temperatur zu einem Objekt mit niedrigerer Temperatur bewegen kann, wenn sich die beiden Objekte berühren oder zusammengebracht werden. Zwei Objekte mit unterschiedlichen Temperaturen lassen Wärme fließen und sich bewegen.
Wenn Sie beispielsweise heißes Wasser und kaltes Wasser mischen, wird das kombinierte Wasser zu warmem Wasser. Sie müssen auch verstehen, dass Temperatur und Hitze zwei verschiedene Dinge sind. Temperatur ist ein Wert, der mit einem Thermometer gemessen werden kann, während Wärme Energie ist, die fließt.
Nach dem Internationalen System (SI) oder MKS ist die Wärmeeinheit Joule (J), während nach CGS die Wärmeeinheit erg ist. Für eine Reihe von Nahrungsmitteln verwendet Hitze die Kalorieneinheit.
Eine Kalorie ist definiert als die Menge an Wärmeenergie, die erforderlich ist, um die Temperatur von 1 Gramm Wasser auf 1 Grad Celsius zu erhöhen. Daraus kann geschlossen werden, dass 1 Kalorie = 4,184 Joule oder allgemein direkt auf 4,2 J aufgerundet wird.
Kalorien Formel
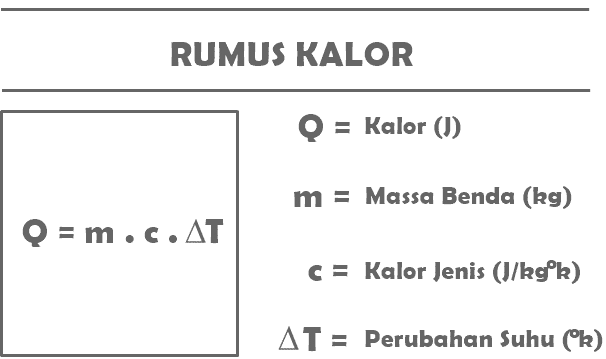
Gemäß der Definition von Wärme, die Sie oben gelesen haben, sind im Folgenden einige der Formeln zusammengefasst, die sich auf Wärmematerial in Physikfächern beziehen.
1. Wärmeübertragungsformel
Q = m. c. T
Mit:
Q = die von einem bestimmten Objekt aufgenommene oder abgegebene Wärmemenge (J)
m = Masse des Objekts, das Wärme aufnimmt oder abgibt (kg)
c = spezifische Stoffwärme (J/kg°C)
T = Temperaturänderung (°C)
2. Spezifische Wärmeformel
Maßstab dieser Formel ist die Wärmeübergangsformel, die wie üblich durch Entfernen des Elements c (spezifische Stoffwärme) mathematisch zu berechnen ist.
c = Q / (m. T)
Mit:
c = spezifische Stoffwärme (J/kg°C)
Q = die von einem bestimmten Objekt aufgenommene oder abgegebene Wärmemenge (J)
m = Masse des Objekts, das Wärme aufnimmt oder abgibt (kg)
T = Temperaturänderung (°C)
3. Wärmekapazitätsformel
C = Q / T
Mit:
C = Wärmekapazität (J/°K)
Q = viel Hitze (J)
T = Temperaturänderung (Kelvin / K)
4. Formel zur Bestimmung der Wärmekapazität
C = m. c
Mit:
C = Wärmekapazität (J/°K)
m = Masse des Objekts, das Wärme aufnimmt oder abgibt (kg)
c = spezifische Stoffwärme (J/kg°K)
5. Schmelzwärme und Dampfformel
Die Formel für die Schmelzwärme lautet wie folgt.
Q = m. L
Die Formel für die Dampfwärme lautet wie folgt.
Q = m. U
Mit:
Q = viel Hitze (J)
m = Masse des Objekts (kg)
L = Schmelzwärme (J/kg)
U = Dampfwärme des Stoffes (J/kg)
Lesen: Thermodynamik
Arten von Kalorien

Es gibt mehrere Arten von Wärme, die anhand des Arbeitsprozesses in einem bestimmten Stoff unterschieden werden. Im Folgenden sind die Arten von Wärme aufgeführt, die Sie verstehen müssen, um ihre Anwendung im täglichen Leben sehen zu können.
1. Bildungswärme (ΔHf)
Die Bildungswärme ist die Wärme, die erzeugt oder benötigt wird, um 1 Mol einer Verbindung in ihren Elementen zu bilden, wie z. B. Gase, die unter Verwendung der Summenformel geschrieben werden. Einige Beispiele für Bildungswärme sind C12, Ö2, Br2, H2.
2. Zersetzungswärme (ΔHd)
Die Zersetzungswärme ist die Form von Wärme, die erzeugt oder benötigt wird, um 1 Mol einer Verbindung in ein anderes Element zu zerlegen.
3. Verbrennungswärme (ΔHc)
Die Verbrennungswärme ist die Wärme, die gewonnen oder benötigt wird, um 1 Mol einer Substanz zu verbrennen, wie z. B. eines Elements oder seiner Verbindung.
4. Neutralisationswärme (ΔHn)
Die Neutralisationswärme ist die Art von Wärme, die erhalten oder benötigt wird, um ein Mol H zu bilden2O aus der Reaktion zwischen einer Säure und einer Base. Diese Wärme ist eine exotherme Reaktion, da es zu einem Temperaturanstieg kommt.
5. Auflösungswärme (ΔHs)
Die Auflösungswärme ist die Art von Wärme, die erzeugt oder benötigt wird, um 1 Mol einer Substanz, die ursprünglich fest war, in einer Lösung aufzulösen.
Lesen: Dichte Formel
Spezifische Wärme und Wärmekapazität
Sie müssen auch wissen, dass Wärme in zwei Substanzen fließen kann, die unterschiedliche Materieteilchen und unterschiedliche Temperaturänderungen haben. Wenn beispielsweise Wasser und Öl auf die gleiche Temperatur erhitzt werden, ändert sich die Temperatur des Öls stärker als die Temperatur des Wassers.
Dies kann passieren, weil in zwei Gegenständen, die zusammengebracht oder zusammengefügt werden, unterschiedliche Wärmearten vorhanden sind. Spezifische Wärme ist die Wärmemenge, die erforderlich ist, um die Temperatur von 1 kg Masse auf 1 °C zu erhöhen, die Einheit ist Kalorien/Gramm °Celsius oder J/kg °C.
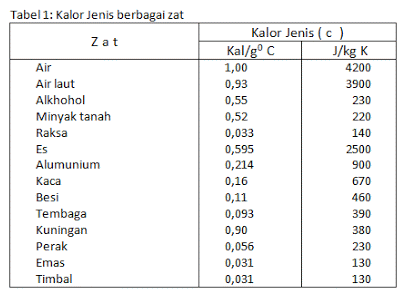
Jede Substanz hat ihre eigene spezifische Wärme und es gibt Unterschiede darin. Der Begriff Wärmekapazität hingegen ist die Wärmemenge, die benötigt oder absorbiert wird, um die Temperatur eines Objekts auf 1 °C zu erhöhen.
Wärmewechsel
Die Wärmeformel funktioniert in ihrer Anwendung nach dem Prinzip, zwei Stoffe, die zusammengebracht oder in Kontakt gebracht werden, zu verändern. Unten ist eine Wärmeänderung, die auftritt, wenn Substanzen zusammengefügt oder zusammengebracht werden.
1. Wärme kann die Temperatur einer Substanz verändern
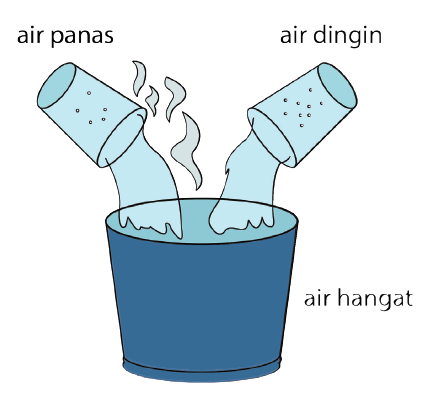
Jedes Basisobjekt hat eine Temperatur, die niedriger als der absolute Nullpunkt ist, also muss das Objekt Wärme haben. Dieser Inhalt bestimmt später, wie viel Wärme die Temperatur des Objekts hat.
Wenn das Objekt erhitzt wird, erhält es zusätzliche Wärme. Die Temperatur wird auch steigen oder steigen. Umgekehrt, wenn das Objekt gekühlt wird, wird Wärme freigesetzt und verursacht einen Temperaturabfall.
2. Hitze kann Stoffe verändern

Bei einigen Arten von Objekten kann das Objekt, wenn es Wärme in bestimmten Einheiten erhält, eine Zustandsänderung erfahren. Wenn zum Beispiel Eis Wärme zugeführt (erhitzt) wird, ändert das Eis seine Form von fest zu flüssig oder sogar gasförmig.
Wenn der Erwärmungsprozess kontinuierlich durchgeführt wird, bewirkt dies, dass sich das Wasser wieder in einen Stoff verwandelt. Dies geschieht, wenn sich das Objekt, das seine Form ändern soll, vom Punkt der Flüssigkeit zum Schmelzpunkt des Objekts bewegt.
Arten der Wärmeübertragung
Nachdem Sie eine Erklärung der Definition, Typen und Formeln von Wärme bis hin zu Wärmeänderungen durchgegangen sind, können Sie feststellen, dass sich Wärme auch bewegen kann, wenn sie auf andere Objekte trifft oder mit ihnen in Kontakt kommt. Im Folgenden sind einige Arten der Wärmeübertragung aufgeführt.
1. Leitung

Die Wärmeübertragung durch Leitung erfolgt beim Durchgang durch eine Zwischensubstanz wie z. B. ein Metall, es folgt jedoch keine permanente Bewegung von Partikeln in der Substanz. Wenn Sie beispielsweise ein Ende eines Metalls erhitzen, wird das andere Ende des Metalls ebenfalls heiß.
Dies liegt an der Wärmeleitung von einer hohen Temperatur zu einer niedrigeren Temperatur. Die erhitzte Metallspitze bewirkt, dass die Metallpartikel Vibrationen in anderen Partikeln erzeugen, die mit ihnen verbunden sind.
Daher schwingen alle Metallpartikel, selbst wenn nur ein Ende des Metalls erhitzt wird, was dann eine Wärmeübertragung verursacht. Ein weiteres Beispiel ist, wenn der Motorradauspuff heiß ist, wenn der Motor eingeschaltet wird.
Wärmeleitung tritt auch auf, wenn Sie das Feuerwerk in Brand halten, den Deckel eines Topfes halten, der sich während des Kochvorgangs heiß anfühlt, Butter, die beim Erhitzen schmilzt, und so weiter. Die Formel für die Wärmeübertragung bei Leitung lautet wie folgt.
Heizrate = Q/t = kA. T / x
2. Konvektion
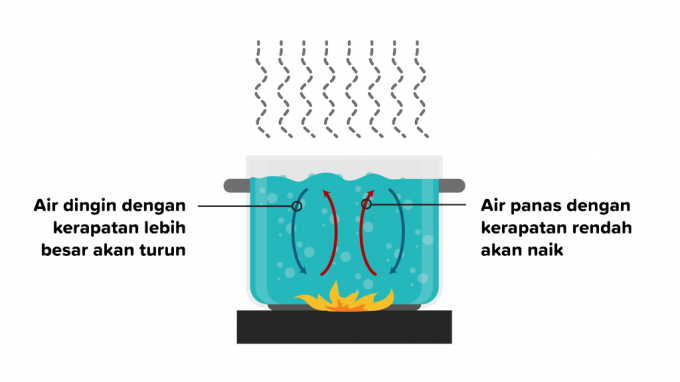
Konvektion ist die Übertragung von Wärme, bei der Wärme einen Stoff durchdringt und die Bewegung von Teilen des Stoffes folgt. Wärmeübertragung durch Konvektion kann in Flüssigkeiten oder Gasen auftreten, daher wird die Konvektion wie folgt in zwei Teile geteilt.
a. Wissenschaftliche Konvektion
Konvektion ist eine Wärmeübertragung, die aufgrund von Auftrieb ohne äußere Faktoren auftritt und durch verschiedene Arten von Objekten beeinflusst wird. Ein Beispielfall ist, wenn Wasser erhitzt wird, bewegt sich die Dichte der heißen Wasserpartikel vom Feuer weg, dann wird es durch eine Wassersubstanz mit niedrigerer Temperatur ersetzt.
b. Erzwungene Konvektion
Anzeige
Konvektion ist eine Wärmeübertragung, die durch den Einfluss äußerer Faktoren wie Druck verursacht wird, sodass die Übertragung gewollt oder erzwungen erfolgt. Das heißt, Wärme wird aufgrund der Hilfe gezwungen, sich an einen Ort zu bewegen.
Beispiele für Fälle sind ein Lüfter, der kalte Luft an einer Stelle erzeugt, die sich heiß anfühlt, das Motorkühlsystem am Autokühler und so weiter.
Eine andere Anwendung der Konvektion tritt beim Erhitzen von Wasser auf, wo es eine Auf- und Abbewegung des Wassers gibt, grüne Bohnensamen das beim Kochen auf und ab geht, der Prozess der Land- und Meeresbrise, die Bewegung von Heißluftballons, Schornsteinrauch Fabrik.
Die Formel für die Wärmeübertragung durch Konvektion lautet wie folgt.
Heizrate = Q/t = hA. T
3. Strahlung

Strahlung ist die Übertragung von Wärme, die keine Zwischensubstanz oder Medium benötigt. Wärmeübertragung durch Strahlung ist nicht dasselbe wie Wärmeleitung und Konvektion. Durch die Strahlungsverschiebung kommen die beiden Substanzen nicht immer in Kontakt oder treffen aufeinander, da Wärme auch ohne Vermittler übertragen werden kann.
Das heißt, Wärme wird von der Wärmequelle selbst in alle Richtungen abgestrahlt und fließt dann in alle erreichbaren Richtungen. Grundsätzlich können alle Gegenstände Wärmestrahlung abgeben und absorbieren, jedoch hängt die Menge von der Temperatur und der Farbe des Stoffes ab.
Je heißer ein Objekt ist als die Umgebungstemperatur, desto mehr Wärme strahlt es an seine Umgebung ab. Wenn also die Oberfläche eines heißen Objekts größer ist, wird die Wärme, die abgestrahlt wird, heißer.
Ein Beispiel für Bestrahlungsfälle im Alltag ist, wenn Sie ein Lagerfeuer machen, wird es sich warm anfühlen Da sich die Feuerquelle in einer bestimmten Entfernung befindet, ist Strahlung zu spüren, wenn die Handflächen bei Annäherung warm werden mit Feuer. Die Wärmeformel für Strahlung lautet wie folgt.
Heizrate = Q/t = eσAT4
4. Wärme isolieren

Wärme hat die Eigenschaft, leicht übertragen zu werden. Sie können verhindern, dass Bewegungen stattfinden, sei es durch Leitung, Konvektion und Strahlung. Zum Beispiel durch Isolierung des Raums; Die Thermoskanne kann die Wassertemperatur heiß oder warm halten, sodass eine Wärmeübertragung verhindert werden kann.
Lesen: Gas-Substanz
Beispiel für ein Kalorienproblem

Die Wärmeformel ist eine Methode, mit der Sie die folgenden Beispielfragen bearbeiten können!
1. Beispielfrage 1
Ein Objekt hat eine Temperatur von 5°C und absorbiert 1500 J Wärme. Die Temperatur des Objekts ändert sich auf 32°C. Berechnen Sie die Wärmekapazität des Objekts!
Lösung:
Q = 1500 J
T = 32 °C – 5 °C = 27 °C = 300 °K
C = Q / T
C=1500/300
C = 5 J/°K
2. Beispielfrage 2
Berechnen Sie die Wärme, die benötigt wird, um 5 kg Wasser von 25 °C auf 105 °C zu erhitzen, wenn bekannt ist, dass die spezifische Wärme von Wasser 1000 J/kg °C beträgt!
Lösung:
m = 5 kg
c = 1000 J/kg°C
T = 105 °C – 25 °C = 80 °C
Q = m. c. T
Q = 5. 1000. 80
Q = 400.000 J
3. Beispielfrage 3
Wenn ein Wasser eine Masse von 3 kg hat und von 30°C auf 100°C erhitzt wird und seine spezifische Wärme 1 J/g°C beträgt, berechnen Sie die für das Wasser benötigte Wärmemenge!
Lösung:
m = 3 kg
c = 1 g/°C = 1000 J/kg°C
T = 100 °C – 30 °C = 70 °C
Q = m. c. T
Q = 3. 1000. 70
Q = 210.000 J
4. Beispielfrage 4
Eine Flüssigkeit hat eine Masse von 5 kg. Die Flüssigkeit benötigt eine Wärme von 200.000 J und wird von 20 °C auf 80 °C erhitzt. Berechnen Sie die spezifische Wärme der Flüssigkeit!
Lösung:
m = 5 kg
Q = 200.000 J
T = 80 °C – 20 °C = 60 °C
c = Q/m. T
c = 200.000 / 5. 60
c = 200.000 / 300
c = 666,67 J/kg°C
5. Beispielfrage 5
Ein Aluminium hat eine Masse von 5 kg. Die Anfangstemperatur beträgt 25°C. Wenn das Aluminium 250.000 J Wärme erhält und seine spezifische Wärme 900 J/kg°C beträgt, berechnen Sie die Endtemperatur des Aluminiums!
Lösung:
m = 5 kg
Q = 250.000 J
c = 900 J/kg°C
T1 = 25 °C
Q = m. c. T
250.000 = 5. 900. (T2 – 25)
T2 – 25 = 250.000 / 5. 900
T2 – 25 = 250.000 / 4.500
T2 – 25 = 55,56
T2 = 55,56 + 25 = 80,56 °C
6. Beispielfrage 6
Dort werden 300 Gramm Wasser mit einer Temperatur von 25 °C mit einer Energie von 1.500 Kalorien erhitzt. Wenn die spezifische Wärme von Wasser 1 cal/g°C beträgt, berechnen Sie die Temperatur des Wassers nach dem Erhitzen!
Lösung:
m = 300 Gramm
T1 = 25 °C
c = 1 cal/g°C
Q = 1.500 kal
Q = m. c. T
1.500 = 300. 1. (T2 – 25)
T2 – 25 = 1500 / 300. 1
T2 – 25 = 5
T2 = 5 + 25 = 30 °C
7. Beispielfrage 7
Es müssen 300 Gramm Wasser von 40°C auf 65°C erhitzt werden. Wenn die spezifische Wärme von Wasser 1 cal/g°C oder 4.200 J/kg°K beträgt, berechnen Sie:
- Viel Wärme wird in Kalorien aufgenommen
- Wie viel Wärme wird in Joule empfangen
Lösung:
m = 300 g = 0,3 kg
T = 65 – 40 = 25 °C
c = 1 cal/g°C = 4.200 J/kg°K
- Kalorien in Kalorien
Q = m. c. T
Q = 300. 1. 25
Q = 7.500 Kalorien
- Wärme in Joule
Q = m. c. T
Q = 0,3. 4.200. 25
Q = 31.500 Kalorien = 132.300 Joule
Basierend auf der obigen Erklärung dreht sich die Wärmeformel nicht nur um das Freigeben und Fordern Wärme, aber es gibt eine Änderung der Wärme, der Wärmeübertragung, sogar der spezifischen Wärme jeder Substanz variieren. Viel Spaß beim Üben und ich hoffe, dieser Artikel ist nützlich!
X SCHLIESSEN
Anzeige
ANZEIGE
X SCHLIESSEN
