Beispiel für ein Molalitätsproblem: Molenbruch, Formel und Lösung
Beispiel eines Molalitätsproblems: Molenbruch, Formel und Lösung – Bei dieser Gelegenheit Über die Knowledge.co.id wird die Molalität anhand mehrerer Beispielfragen und natürlich anderer Dinge, die sie ebenfalls abdecken, diskutieren. Schauen wir uns die Diskussion im folgenden Artikel gemeinsam an, um sie besser zu verstehen.
Beispiel für ein Molalitätsproblem: Molenbruch, Formel und Lösung
Molalität oder Molkonzentration ist ein Maß für die Konzentration eines gelösten Stoffes in einer Lösung, ausgedrückt als Stoffmenge in einer bestimmten Masse des Lösungsmittels. Dies unterscheidet sich von der Definition der Molarität, die auf einem bestimmten Lösungsvolumen basiert.
Die in der Chemie übliche Molalitätseinheit ist Mol/kg. Eine Lösung mit einer Konzentration von 1 mol/kg wird manchmal auch als 1 molal ausgedrückt. Der Begriff Molalität wird in Analogie zur Molarität gebildet, die die molare Konzentration einer Lösung angibt.
Die Molalität einer Lösung kann durch Zugabe von etwas Lösungsmittel getestet werden. Einfacher ausgedrückt ist die Molalität (m) einer Lösung die Molzahl des gelösten Stoffes dividiert durch die Kilogramm Lösungsmittel. Molalität oder Molalität ist die Konzentration einer Lösung, die die Anzahl der Mol (n) des gelösten Stoffes in 1 kg oder 1000 Gramm Lösungsmittel angibt.
Der Unterschied zwischen Molalität und Molarität besteht darin, dass Molalität Molalität oder Molkonzentration (m) die Anzahl der Mol ausdrückt gelöster Stoff in 1000 Gramm Lösungsmittel, während die Molarität eine Aussage über die Anzahl der Mol gelösten Stoffs in jedem Liter ist Lösung. Die Molarität wird durch die Notation M dargestellt und die Einheiten sind Mol/Liter.
Molalitätsformel
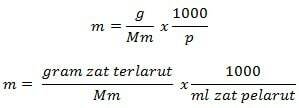
Information
m = Molalität (mol/kg)
g = Gramm gelöster Stoff (g)
Mm = Molmasse der Substanz (g/mol)
P = Masse des Lösungsmittels (g)
Molalitätsbeziehung mit Massenprozent
Massenprozent ist eine Konzentrationseinheit, die üblicherweise in chemischen Lösungen verwendet wird. Beispiele für Lösungen, die wir jeden Tag finden können, sind 75 %ige Alkohollösung und 24 %ige Essigsäurelösung. Massenprozent ist die Anzahl der Gramm gelöster Substanz in 100 Gramm Lösungsmasse. Die Gleichung, die die Berechnung des Massenprozentsatzes zeigt, lautet wie folgt:

Beziehung zwischen Molalität und Molarität
Die Molarität drückt die Anzahl der Mol gelösten Stoffes in einem Liter Lösung aus. Die Molarität kann in Molalität umgewandelt werden, indem das Volumen der Lösung in die Masse der Lösung umgerechnet wird. Für die Umrechnung von Volumen in Masse sind Daten zur Dichte der Lösung (p) erforderlich, die sich wie folgt formulieren lassen:

Molenfraktion
Der Molenbruch ist ein Maß für die Konzentration einer Lösung und drückt das Verhältnis der Molzahl in einem Teil einer Substanz zur Gesamtmolzahl in den Bestandteilen der Lösung aus. Der Stoffmengenanteil wird in 2 Teile geteilt:
Molenbruch gelöster Stoffe (Xt)
Die Formel für den Stoffmengenanteil des gelösten Stoffes (Xt), nämlich:

Information:
Xt = Molenbruch des gelösten Stoffes
Nt = Anzahl der Mole des gelösten Stoffes
Np = Anzahl der Mol Lösungsmittel
Molenbruch des Lösungsmittels (Xp)
Die Formel für den Molenbruch des Lösungsmittels (Xp), nämlich:

Information
Xp = Molenbruch des Lösungsmittels
Nt = Anzahl der Mole des gelösten Stoffes
Np = Anzahl der Mol Lösungsmittel
Die Summe der Stoffmengenanteile von gelöstem Stoff und Lösungsmittel beträgt 1
Xt + Xp = 1
Beispiele für Molalitätsprobleme und Lösungen
Problem 1
Wie groß ist die Molalität einer Lösung, die 4 g NaOH (Ar Na = 23 g/mol, Ar O = 16 g/mol und Ar H = 1 g/mol) enthält, gelöst in 250 g Wasser?
Fertigstellung:
Ist bekannt:
Masse NaOH = 4 gr
ArNa = 23 g/mol
ArO = 16 g/mol
ArH = 1 g/mol
Wassermasse = 250 g = 0,25 kg
Gefragt: m = ?
Antwort:
Herr. NaOH = 40 g/mol
Anzahl der Mol NaOH = Masse/Mr
Anzahl der Mol NaOH = 4 g/(40 g/mol)
Anzahl der Mol NaOH = 0,1 Mol
m = Anzahl der Mol/p
m = 0,1 mol / 0,25 kg
m = 0,4 m
Problem 2
Wie groß ist die Molalität einer 37 %igen HCl-Lösung? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol)
Fertigstellung:
Ist bekannt:
Masse an HCl = 37 %
ArH = 1 g/mol
ArCl = 35,5 g/mol
Gefragt: m = ?
Antwort:
Herr. HCl = 36,5 g/mol
Angenommen, die Masse der Lösung beträgt 100 Gramm, dann beträgt die Masse von HCl:
HCl-Masse = 37 % x 100 g
Masse an HCl = 37 gr
Masse des Lösungsmittels = Masse der Lösung – Masse HCl
Masse des Lösungsmittels = 100 g – 37 g
Masse des Lösungsmittels = 63 g = 0,063 kg
Anzahl der Mole HCl = Masse/Mr
Anzahl der Mole HCl = 37 g/(36,5 g/mol)
Anzahl der Mol HCl = 1,01 Mol
m = Anzahl der Mol/Masse des Lösungsmittels
m = 1,01 mol/0,063 kg
m = 16,03 m
Problem 3
Bestimmen Sie die Molalität der Lösung, die durch Auflösen von 12 Gramm Harnstoff CO(NH2)2 in 250 Gramm Wasser hergestellt wird.
Fertigstellung:
Ist bekannt:
Masse Harnstoff = 12 gr
Herr Harnstoff = 60 g/mol
Masse des Lösungsmittels = 250 g = 0,25 kg
Gefragt: m = ?
Werbung
Antwort:
Molzahl Harnstoff = Masse/Mr
Molzahl Harnstoff = 12 g/(60 g/mol)
Molzahl Harnstoff = 0,2 Mol
m = Anzahl der Mol/Masse des Lösungsmittels
m = 0,2 mol / 0,25 kg
m = 0,8 m
Problem 4
Wie groß ist die Molalität einer alkoholischen Lösung mit 23 Masse-% Ethanol (Mr = 46)?
Antwort:
Ist bekannt:
Masse Ethanol = 23 %
Mr Ethanol = 46 g/mol
Gefragt: m = ?
Fertigstellung:
Beispielsweise beträgt die Masse der Alkohollösung 100 Gramm, dann beträgt die Masse des Ethanols:
Masse Ethanol = 23 % x 100 g
Masse Ethanol = 23 gr
Masse des Lösungsmittels = Masse der Lösung – Masse Ethanol
Masse des Lösungsmittels = 100 g – 23 g
Masse des Lösungsmittels = 77 g = 0,077 kg
Anzahl der Mol Ethanol = Masse/Mr
Anzahl der Mol Ethanol = 23 g /(46 g/mol)
Molzahl Ethanol = 0,5 Mol
m = Anzahl der Mol/Masse des Lösungsmittels
m = 0,5 mol/0,077 kg
m = 6,49 m
Problem 5
Berechnen Sie die Konzentration (Massen-%) von Glucose in einer 2 molalen Glucoselösung.
Fertigstellung:
Ist bekannt:
m = 2 molal = 2 mol/kg = 0,002 mol/gr
Mr Glucose = 180 g/mol
Fragte: Masse an Glukose (%) = ?
Antwort:
Mol Glucose = Masse/Mr
Mol Glucose = Masse Glucose/(180 g/mol)
Mol Glucose = Glucosemasse x 0,005 Mol/g
Setze die Mol Glucose in die folgende Gleichung ein:
m = Mol Glucose/Masse Lösungsmittel
0,002 = Masse Glucose x 0,005/Masse Lösungsmittel
o, oo2/o, oo5 = Masse Glucose/Masse Lösungsmittel
2/5 = Masse Glucose/Masse Lösungsmittel
Das Massenverhältnis von Glucose: Masse des Lösungsmittels = 2:5, während das Massenverhältnis von Glucose: Masse der Lösung = 2:7 ist.
Also,
% Masse an Glukose = (Masse an Glukose/Masse der Lösung) x100 %
Massenprozent Glucose = (2/7) x 100 %
% Glukosemasse = 28,57 %
Problem 6
Wie groß ist die Molalität einer Lösung, die 8 g NaOH (Ar Na = 23 g/mol, Ar O = 16 g/mol und Ar H = 1 g/mol) enthält, gelöst in 250 g Wasser?
Diskussion
Ist bekannt:
Masse NaOH = 8 gr
ArNa = 23 g/mol
ArO = 16 g/mol
ArH = 1 g/mol
Wassermasse = 250 g = 0,25 kg
Gesucht: Molalität (m)….?
Antwort:
Herr. NaOH = 40 g/mol
Die Anzahl der Mol NaOH = Masse/Mr
Anzahl der Mole NaOH = 8 g/(40 g/mol)
Die Anzahl der Mol NaOH = 0,2 Mol
m = Anzahl der Mol/p
m = 0,2 mol / 0,25 kg
m = 0,8 m
Problem 6
Bestimmen Sie die Molalität der Lösung, die durch Auflösen von 15 Gramm Harnstoff CO(NH2)2 in 250 Gramm Wasser hergestellt wird.
Diskussion
Ist bekannt:
Harnstoffmasse = 15 gr
Herr Harnstoff = 60 g/mol
Lösungsmittelmasse = 250 g = 0,25 kg
Gesucht: Molalität (m)…. ?
Antwort:
Anzahl der Mol Harnstoff = Masse/Mr
Gesamtmole Harnstoff = 15 g / 60 g/mol
Die Anzahl der Mol Harnstoff = 0,25 Mol
m = Anzahl der Mol/Masse des Lösungsmittels
m = 0,25 mol / 0,25 kg
m = 1 m
Problem 7
Wie groß ist die Molalität einer 37 %igen HCl-Lösung? (Ar H = 1 g/mol, Ar Cl = 35,5 g/mol).
Diskussion
Ist bekannt:
Masse an HCl = 37 %
ArH = 1 g/mol
ArCl = 35,5 g/mol
Gesucht: Molalität (m)…?
Antwort:
Herr. HCl = 36,5 g/mol
Angenommen, die Masse der Lösung beträgt 100 Gramm, dann beträgt die Masse von HCl:
HCl-Masse = 37 % x 100 g
Masse an HCl = 37 gr
Masse des Lösungsmittels = Masse der Lösung – Masse HCl
Masse des Lösungsmittels = 100 g – 37 g
Masse des Lösungsmittels = 63 g = 0,063 kg
Anzahl der Mole HCl = Masse/Mr
Anzahl der Mole HCl = 37 g/(36,5 g/mol)
Anzahl der Mol HCl = 1,01 Mol
m = Anzahl der Mol/Masse des Lösungsmittels
m = 1,01 mol/0,063 kg
m = 16,03 m

Aufgabe 8
Bestimmen Sie die Menge (Gramm) NaOH, die in 1 Liter Wasser gelöst werden muss (Wasser = 1,00 g/ml), um 0,25 m NaOH zu erhalten.
Diskussion
Ist bekannt:
1 l Wasser = 1000 ml = 1000 g (da ρ Wasser = 1,00 g/ml)
mNaOH = 0,25 m
Herr NaOh = 40
Gefragt: gr…?
Antwort:
mNaOH = gr / Mr x 1.000 / P
0,25 = gr/40 x 1.000/1.000
0,25 = g/40
g = 0,25 x 40
g = 10 Gramm
Die benötigte Menge NaOH beträgt also 10 Gramm.
Problem 9
Bestimmen Sie, wie viele ml Wasser benötigt werden, um 4,9 Gramm H2SO4 mit einer Konzentration von 0,25 M aufzulösen (Ar H = 1; S = 32; O =16)!
Diskussion
Ist bekannt:
mH2SO4 = 0,25
Herr H2SO4 = 98
gr = 4,9 Gramm
Gefragt :p???
Antwort:
m = gr/Herr x 1.000/P
0,25 = 4,9/98 x 1.000/P
p = 20 Gramm (20 ml)
Das Wasservolumen beträgt also 20 ml.
Aufgabe 10
Welche Wassermasse wird benötigt, um eine 1,2 m Lösung mit 0,6 mol NaCl herzustellen?
Diskussion
Molalität (m) = 1,2 mm =
NP
1,2 =
0,6P
P=
0,61,2
= 0,5 kg
Die benötigte Wassermasse (Lösungsmittelmasse) beträgt also 0,5 kg
Aufgabe 11
Angenommen, in 1 Liter Lösungsmittel sind 2 Mol gelöster Stoff gelöst. Wie groß ist die Molalität?
Diskussion
gelöste Mole (n) = 2 molm =
NP
m =
21
= 2m
Berechnen Sie die Molalität von 25 Gramm KBr (Mr = 119), gelöst in 750 ml reinem Wasser.
Diskussion
gelöster Stoff = 25 Gramm
Herr = 119
Lösungsmittel (P) = 750 ml = 750 Gramm (weil ρ Wasser = 1,00 g/ml) = 0,75 kgn =
gelöster StoffHerr
n =
25119
= 0,21 mol
m =
NP
m =
0,210,75
= 0,28 m
So die Rezension von Über die Knowledge.co.id um Beispiel eines Molalitätsproblems , Hoffentlich kann ich Ihre Einsichten und Ihr Wissen erweitern. Vielen Dank für Ihren Besuch und vergessen Sie nicht, andere Artikel zu lesen.
Inhaltsverzeichnis
Empfehlung:
- Cellulose ist: Definition, Typ, Struktur, Eigenschaften und… Cellulose ist: Definition, Typ, Struktur, Eigenschaften und Funktionen – Cellulose ist eine faserartige Verbindung und kommt in den schützenden Zellwänden von Pflanzen vor. Um es besser zu verstehen, werden wir natürlich darüber diskutieren ...
- √ Definition der Ausdehnung in Länge, Formel, Fläche und Volumen eines Stoffes… Definition der Längenausdehnung, Formeln, Fläche und Volumen von Festkörpern – In dieser Diskussion werden wir die Längenausdehnung erläutern. Dazu gehören der Begriff der langen Expansion, lange Expansionsformeln, Fläche, Volumen der Materie ...
- Maße: Definition, Umrechnung von Längeneinheiten, Anleitung ... Messleiter: Definition, Umrechnung von Längeneinheiten, Verwendung und Beispielfragen – Was ist drin? Was meinst du mit Größenleiter und wie benutzt man sie? Dieses Mal wird es Knowledge.co.id geben besprechen Sie es...
- Kovalente Bindungen: Definition, Eigenschaften, Typen, Formeln ... Kovalente Bindungen: Definition, Eigenschaften, Typen, chemische Formeln und Eigenschaften von Verbindungen – Was ist eine kovalente Bindung? Bei dieser Gelegenheit wird Seputarknowledge.co.id darüber und natürlich auch über andere Dinge diskutieren deckte es ab. Lassen…
- Umweltsprache: Definition, Zweck, Merkmale und… Umweltrede: Definition, Zweck, Merkmale und Beispiele – Wie ist der Text der Umweltrede aufgebaut? Was ist gut und richtig? Bei dieser Gelegenheit wird Seputarknowledge.co.id darüber und natürlich über Dinge diskutieren Welche…
- Kegelformeln, Merkmale, Eigenschaften, Elemente und Problembeispiele Kegelformeln, Eigenschaften, Eigenschaften, Elemente und Beispiele Problem – Wie berechnet man die Fläche und das Volumen einer Form? Kegelraum?, Bei dieser Gelegenheit wird Seputarknowledge.co.id darüber und natürlich über andere Dinge diskutieren Welche…
- Viskositätsformel: Definition von Viskosität, Koeffizient und… Viskositätsformel: Viskositätsdefinition, Koeffizient und Einflussfaktoren – Wie lautet die Viskositätsformel? Ist es? Die Viskosität ist ein Maß für den Widerstand einer Flüssigkeit, der sich entweder durch Belastung oder durch … ändert Druck. Bei dieser Gelegenheit hat Seputarknowledge.co.id…
- Gewichtseinheit: Definition, Umrechnungsleiter und Beispiele… Gewichtseinheit: Definition, Umrechnungsleiter und Problembeispiele – Was ist eine Gewichtseinheit?, Aus diesem Anlass Über das Knowledge.co.id wird darüber gesprochen, inklusive Verständnis und natürlich auch über andere Dinge deckte es ab. Lassen…
- Trägheitsmoment: Definition, Faktoren, Formengleichungen… Trägheitsmoment: Definition, Faktoren, Gleichungen in Objektformen und Beispielprobleme – Was gemeint ist Mit dem Trägheitsmoment?, Bei dieser Gelegenheit wird Se über das Wissen.co.id darüber sprechen und natürlich darüber Gegenstand…
- Gleichmäßig wechselnde Kreisbewegung: Definition, Größe… Gleichmäßig wechselnde Kreisbewegung: Definition, physikalische Größe, Formeln und Problembeispiele – Was ist Bewegung? Regelmäßige Änderungen und Beispiele? Bei dieser Gelegenheit wird Seputarknowledge.co.id darüber diskutieren und natürlich über...
- Unbestimmtes Integral: Definition, Formeln, Eigenschaften und Beispiele… Unbestimmtes Integral: Definition, Formeln, Eigenschaften und Beispiele für Probleme – Was ist mit unbestimmtem Integral gemeint? Natürlich und wie berechnet man die mathematischen Operationen? Wille…
- Definition von Lernmethoden: Merkmale, Zweck, Typen und… Definition von Lernmethoden: Merkmale, Zweck, Typen und Diskussion – Was ist mit Methode gemeint? Lernen?, bei dieser Gelegenheit wird Seputarknowledge.co.id darüber und natürlich über andere Dinge diskutieren Auch…
- Chemisches Gleichgewicht: Definition, Gesetze, Formeln, Beispielprobleme Chemisches Gleichgewicht: Definition, Gesetze, Formeln, Beispielprobleme – In dieser Diskussion werden wir es erklären über chemisches Gleichgewicht, Formelgesetz und ausgestattet mit Beispielen für chemisches Gleichgewicht mit vollständigem und...
- Säure-Base-Lösungen: Definition, Säure-Base-Theorie, Eigenschaften und… Säure-Base-Lösungen: Definition, Säure-Base-Theorie, Eigenschaften und Typen – Säure- und Basenlösungen sind zwei Gruppen chemischer Verbindungen, die im täglichen Leben weit verbreitet sind und verwendet werden.
- Bauraum – Definition, Formeln und verschiedene… Raum bauen – Definition, Formeln und ihre verschiedenen Typen – Bei dieser Gelegenheit möchten wir mathematisches Material über geometrische Formen besprechen, sowohl aus dem Verständnis als auch von anderen. Lassen Sie uns sofort besprechen...
- √ Säure-Base-Indikator: Definition, Typen und Beispiele Säure-Base-Indikatoren: Definition, Typen und Beispiele – Bei dieser Gelegenheit wird Around Knowledge über Säure-Base-Indikatoren diskutieren. Was in dieser Diskussion die Bedeutung des Säureindikators erklärt ...
- Boyles Gesetz: Definition, Formeln, Anwendungen und Beispiele… Boyles Gesetz: Definition, Formeln, Anwendungen und Beispiele für Probleme – In dieser Diskussion werden wir das Gesetz von Boyle erläutern. Dazu gehören die Bedeutung des Boyle-Gesetzes, die Formel des Boyle-Gesetzes, die Anwendung von ...
- Motivierende Kurzgeschichten: Definition, Schreibtipps und Beispiele Motivierende Kurzgeschichten: Definition, Schreibtipps und Beispiele – Was ist eine motivierende Kurzgeschichte?, On Bei dieser Gelegenheit wird Seputarknowledge.co.id diskutieren, ob es sich um die Kurzgeschichte der Freundschaft und andere Dinge handelt darüber. Mal sehen…
- Definition von Druck: Druckarten, Formeln und Beispielprobleme Definition von Druck: Druckarten, Formeln und Beispielaufgaben – Was ist Druck? Bei Bei dieser Gelegenheit werden wir rund um Knowledge.co.id diskutieren, was Druck ist und welche anderen Elemente es gibt deckte es ab. Mal sehen…
- Dynamische Flüssigkeiten: Typen, Merkmale, Bernoulli-Gleichung, Theoreme ... Dynamische Flüssigkeiten: Typen, Eigenschaften, Bernoulli-Gleichung, Toricelli-Theorem, Formeln und Beispiele für Probleme – Was ist das? dynamische Flüssigkeiten und ihre Typen? um…
- Dichte von Wasser: Definition, Formeln und Beispiele Dichte von Wasser: Definition, Formeln und Beispiele – Was ist die Dichte von Wasser? Lasst uns gemeinsam sehen…
- Definition von Menge, Einheit, Maß und Beispielen… Definition von Menge, Einheit, Maß und Beispielen (vollständig) – In grundlegenden physikalischen Konzepten haben wir sicherlich etwas kennengelernt, das mit dem Alltagsleben zu tun hat. Wie Messen der Höhe, Wiegen der Masse, Messen der Breite, ...
- Beispiele wissenschaftlicher Arbeit: Funktionen und Regeln der Sprache Beispiele für wissenschaftliche Arbeiten: Funktionen und Regeln der Sprache - Was sind Beispiele für gute und korrekte Formen des Verfassens wissenschaftlicher Arbeiten? Zuvor hat Seputar the Knowledge.co.id über wissenschaftliche Arbeit gesprochen: Definition, Eigenschaften, Vorteile,…
- Beispiele für flache Formen: Typen, Eigenschaften und Formeln von flachen Formen Beispiele für flache Formen: Typen, Eigenschaften und Formeln von flachen Formen – Was sind die Beispiele für flache Formen?
- Beispielfragen zum Sportunterricht für Klasse 11 (XI), SMA/MA/SMK, Semester 1 und 2 Beispiele für Sportfragen für Klasse 11 (XI) für SMA/MA/SMK Semester 1 und 2 (2019 und 2020) – Bei dieser Gelegenheit wird Seputarknowledge.co.id Beispiele für Sportfragen für Klasse 11 Multiple Choice und Essay diskutieren ...
- Niederschlag ist: 12 Definitionen nach Experten, Arten,… Niederschlag ist: 12 Definitionen nach Expertentypen und Faktoren – In dieser Diskussion wird Around Knowledge das Thema Niederschlag erläutern. Niederschlag ist ein klimatisches Ereignis, das natürlich ist,...
- √ Definition chemischer Verbindungen, Eigenschaften, Typen und Nomenklatur… Definition chemischer Verbindungen, Eigenschaften, Typen, vollständige Nomenklatur – In dieser Diskussion werden wir chemische Verbindungen erläutern. Behandelt die Definition, Eigenschaften, Typen und Nomenklatur chemischer Verbindungen mit Diskussion...
- Einzelstoffe sind: Definition, Elemente und Verbindungen Einzelstoffe sind: Definitionen, Elemente und Verbindungen – Was bedeutet ein einzelner Stoff? Schauen wir uns die Diskussion gemeinsam an...
- Schiefe Ebene: Definition, Formeln, mechanischer Vorteil und… Schräge Ebene: Definition, Formeln, mechanische Vorteile und Beispiele für Probleme – Was ist mit Ebene gemeint? schräg und wie berechnet man die Physik? natürlich…
- Einheitenumrechnung: Definition, Faktor, Länge, Masse, Zeit,… Einheitenumrechnung: Definition, Faktor, Länge, Masse, Zeit, Volumen und Druck – Was ist Einheitenumrechnung?, Bei dieser Gelegenheit wird Seputarknowledge.co.id darüber diskutieren, einschließlich Faktoren, Typen und natürlich anderer Dinge Welche…
