المركبات: التعريف ، الأنواع ، الأمثلة
جار التحميل...
دون أن يدركوا ذلك ، غالبًا ما يتعامل البشر مع أنواع مختلفة من المركبات في الحياة اليومية. على الرغم من أنه ربما لا يدرك الجميع ، ناهيك عن فهم معنى المركب. في الواقع ، هناك العديد من الأمثلة على المركبات التي توجد غالبًا ، مثل الملح والسكر والماء وما إلى ذلك.
بشكل عام ، يتم تصنيف المركبات إلى عدة أنواع بناءً على العناصر المكونة. بينما تتم عملية تحلل المركبات من خلال تفاعل كيميائي. كما أنه يميز شكل وملمس وطعم ورائحة كل نوع من المركبات.
قائمة المحتويات
تسمية الصيغ المركبة
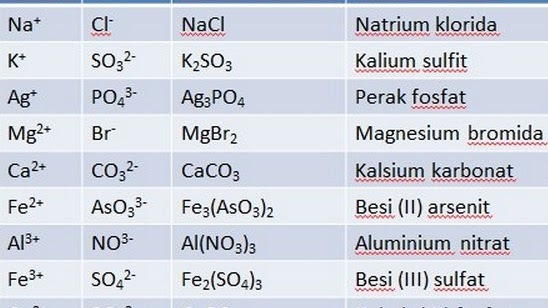
المركب هو مادة واحدة يمكن تقسيمها إلى مادتين أو أكثر من خلال تفاعل كيميائي. مثال على المركب الذي يوجد غالبًا في الحياة اليومية هو الماء. في هذه العملية ، الماء عبارة عن مزيج من عنصري الأكسجين (O) والهيدروجين (H) مع الصيغة الكيميائية H20.
وفقًا للتقرير من الموقع الرسمي لوزارة التعليم والثقافة في جمهورية إندونيسيا ، يُذكر أن أصغر جزء من العنصر هو الذرة. إذا اتحدت ذرتان من خلال تفاعل كيميائي ، فستشكل جزيءًا أو أصغر جزء من المركب.
وفي الوقت نفسه ، عملية تكوين المركبات من خلال الخلط الكيميائي والتحلل الحراري أو الكهربائي. المركبات لها خصائص مختلفة عن العناصر المكونة لها.
على سبيل المثال ، تختلف خصائص الماء عن خصائص العناصر المكونة له ، وهي الأكسجين وغاز الهيدروجين. كما أن الاختلاف في المظهر حقيقي جدًا. لأن الماء سائل ، والهيدروجين غاز. بالإضافة إلى ذلك ، يمكن استخدام المياه لإطفاء الحرائق.
ومع ذلك ، فإن الهيدروجين مادة قابلة للاشتعال. بينما الأكسجين مادة لازمة في عملية الاحتراق. لذلك ، يمكن ملاحظة أن العناصر المكونة والمركبات الناتجة لها خصائص وأشكال ووظائف معاكسة للغاية.
إذن ، ما هو الفرق بين المركب والمزيج والعنصر؟ على الرغم من أن المركبات والعناصر عبارة عن مواد منفردة. ومع ذلك ، هناك اختلافات بين المركبات والعناصر وكذلك الخلائط.
هذا لأن العنصر عبارة عن مادة واحدة لا يمكن تحويلها إلى مواد أبسط ، وسيظل العنصر محتفظًا بخصائصه أو خصائصه الأصلية.
مثال على العناصر:
- ذهب
- قيادة
- حديد
- نحاس
- الزنك
- نيكل
الخليط عبارة عن مادة تتكون من مادتين أو أكثر ، لكنها لا تزال تتمتع بخصائص المادة الأصلية. تتضمن أمثلة المخاليط ما يلي:
- هواء
- ماء النهر
- صخر
- حليب الشوكولاتة
- ملح اليود
- قهوة
- شاي حلو
اقرأ: سائل
أنواع الكمبوندات
قبل مناقشة المزيد حول الأمثلة المطلقة للمركبات في الحياة اليومية. إنه لأمر جيد إذا كان بإمكانك أيضًا التمييز بين أنواع المركبات.
بناءً على العناصر المكونة ، يتم تصنيف المركبات إلى عدة أنواع ، وهي على النحو التالي:
1. مركب عضوي

يأتي من الكائنات الحية وعملية التمثيل الضوئي. تحتوي المركبات العضوية على عنصر الكربون (C) باعتباره السلسلة الرئيسية. هذا النوع من المركبات العضوية له الخصائص المميزة لكونه غير قابل للذوبان في الماء ، وقابل للذوبان فقط إذا تم خلطه بالمذيبات العضوية.
نظرًا لأنه يتكون من عنصر الكربون (C) ، فإنه يتسبب في أن تكون المركبات العضوية أكثر قابلية للاشتعال. مثال على مركب عضوي السكر (C12H22011)
2. مركب غير عضوي
الإعلانات

هذا النوع من المركب يأتي من الموارد المعدنية. تحتوي المركبات غير العضوية على نقاط غليان أعلى نسبيًا من المركبات العضوية. ومع ذلك ، تميل المركبات غير العضوية إلى أن تكون غير قابلة للاشتعال وقابلة للذوبان في الماء بسهولة. على سبيل المثال ، ثاني أكسيد السيليكون (SiO2).
3. حامِض

الجزيئات التي يمكنها التبرع بأيونات الهيدروجين H+ ويشكل رابطة تساهمية مع حمض لويس. في الكيمياء ، تتكون المركبات الحمضية من ثلاثة تعريفات ، وهي Arrhenius و Bronsted-Lowry و Lewis.
بشكل عام ، للأحماض الخصائص التالية:
- تعكر عندما تذوب في الماء.
- يتفاعل بعنف عند مزجه بالمعادن.
- يلمس اللمس ولديه القدرة على إتلاف الجلد.
- تحتوي على درجة حموضة أقل من 7.
- الأحماض هي إلكتروليتات وإن لم تكن بالضرورة أيونية.
- يمكن تحويل ورق عباد الشمس الأزرق إلى اللون الأحمر.
للأحماض مجموعة متنوعة من الاستخدامات ، بما في ذلك إزالة الصدأ من الأجسام المعدنية من خلال التخليل أو التخليل. بالإضافة إلى ذلك ، يمكن أيضًا استخدام الحمض كمحلول إلكتروليت في بطاريات الخلايا الرطبة. يمكن استخدام حامض الكبريتيك كعامل مساعد لصنع البنزين.
اقرأ: قاعدة حمضية
4. المركبات الأيونية

يشير هذا المصطلح إلى مركب كيميائي يتكون من أيونات مرتبطة ببعضها البعض كهروستاتيكيًا (روابط أيونية). على الرغم من أن هذا المركب محايد بشكل عام ، إلا أنه يتكون من أيونات موجبة الشحنة (كاتيونات) وأيونات سالبة الشحنة (الأنيونات) ، سواء على شكل صوديوم أو كلوريد أو كربونات.
خصائص المركبات الأيونية:
- تتميز بدرجة غليان عالية جدًا مع ضغط بخار منخفض.
- القلوية أو التشابه مع المركبات الحمضية.
- معظم أنواع المركبات الأيونية هشة للغاية.
- يتم تحديد انضغاطية المركبات الأيونية من خلال الهيكل.
- سهل الذوبان في السوائل القطبية ، مثل الماء. ومع ذلك ، فإنه يميل إلى أن يكون من الصعب إذابته في البنزين.
- الموصلية المنخفضة وعموما لا توصل كهرباء كبيرة.
للمركبات الأيونية مجموعة متنوعة من الاستخدامات ويشيع استخدامها من قبل الناس في الحياة اليومية. تتضمن أمثلة المركبات الأيونية حليب المغنيسيا والبوراكس والجير المطفأ.
5. ملح

في الكيمياء ، يصنف الملح إلى مركبات أيونية تتكون من أيونات سالبة (أنيونات) وأيونات موجبة (كاتيونات) ، وبالتالي تشكل مركبات بدون شحنة أو متعادلة. يتكون الملح من تفاعل القواعد والأحماض ، مثل الكلوريد ، والأسيتات ، والفلوريد ، والكبريتات ، وكلوريد الصوديوم.
من بين جميع أنواع الملح الموجودة ، لكل ملح طعم مختلف ، وهي:
- حلو (رصاص وخلات)
- مالح (كلوريد الصوديوم)
- حمض (بيطرطرات البوتاسيوم)
- مالح (جلوتامات أحادية الصوديوم)
- المر (كبريتات المغنيسيوم).
6. أكسيد
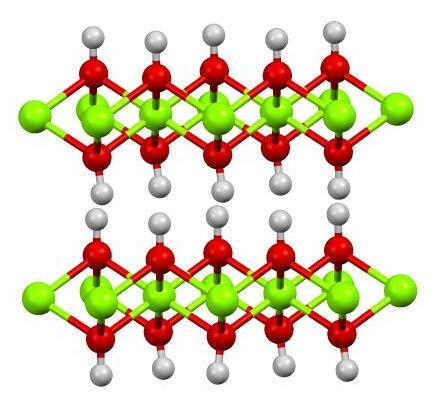
تحتوي مركبات الأكسيد على ذرات الأكسجين وعناصر أخرى. هل تعلم أن معظم قشرة الأرض تتكون من أكاسيد؟ تتشكل هذه المركبات عندما تتأكسد العناصر بالأكسجين. تميل الأكاسيد إلى أن يكون لها هياكل أيونية ذات نقاط غليان عالية.
7. لغة

المركبات التي تمتص أيونات الهيدرونيوم (H3س) عندما يذوب في الماء. القاعدة عبارة عن ثنائي من عنصر حمضي أو كيميائي يحتوي على درجة حموضة أكبر من 7. بشكل عام ، تنقسم القواعد إلى نوعين ، وهما القواعد الضعيفة والقواعد القوية. يعتمد على قدرته على إطلاق أيونات OH.
القواعد لها بعض الخصائص المشتركة ، وهي كما يلي:
- له طعم مر.
- ملمس قاعدي ناعم مثل الصابون.
- يمكن تغيير لون عباد الشمس الأحمر إلى اللون الأزرق.
- قادرة على إجراء التيار الكهربائي.
- يمكن أن تحيد الأحماض.
- أسباب التجوية.
- قيمة الأس الهيدروجيني تتجاوز الرقم 7.
اقرأ: صلب
أمثلة على المركبات في الحياة اليومية

في الحياة اليومية ، لا يمكن فصل الكائنات الحية عن المركبات. علاوة على ذلك ، هناك العديد من المركبات التي يستهلكها الإنسان للبقاء على قيد الحياة.
فيما يلي أمثلة على المركبات التي يستخدمها البشر غالبًا:
| مثال مركب | صيغة كيميائية |
| غاز أول أكسيد الكربون | كو |
| غاز ثاني أكسيد الكربون | كو2 |
| غاز أول أكسيد النيتروجين | رقم |
| ماء | ح2ا |
| ملح المطبخ | كلوريد الصوديوم / كلوريد الصوديوم |
| حامض الهيدروكلوريك | HCI |
| حامض الكبريتيك | ح2لذا4 |
| حمض الخليك (الخل) | CH3COOH |
| غاز الأمونيا | نيو هامبشاير3 |
| هيدروكسيد الصوديوم | هيدروكسيد الصوديوم |
| سكر | C12H22011 |
| اليوريا | ثاني أكسيد الكربون (NH2) 2 |
| كحول | C2H3OH |
| الكالسيوم | كاكو 3 |
من خلال معرفة أمثلة المركبات وأنواعها. يمكنك الآن فهم نوع المركبات الموجودة في الأطعمة والمشروبات والأشياء المستخدمة يوميًا بشكل أفضل. لذلك ، يمكنك أيضًا أن تكون أكثر حرصًا في اختيار ما تستهلكه وتستخدمه.
X اغلاق
الإعلانات
الإعلانات
X اغلاق
