مثال على مشكلة مولية: الكسر الجزيئي والصيغة والحل
مثال مشكلة مولية: الكسر الجزيئي والصيغة والحل - في هذه المناسبة حول Knowledge.co.id سيناقش موضوع المولودة بالعديد من الأمثلة للأسئلة وبالطبع حول أشياء أخرى تغطيها أيضًا. دعنا نلقي نظرة على المناقشة معًا في المقالة أدناه لفهمها بشكل أفضل.
مثال على مشكلة مولية: الكسر الجزيئي والصيغة والحل
تركيز مولالي أو مولال هو مقياس لتركيز المذاب في محلول من حيث كمية المادة في كتلة معينة من المذيب. هذا يختلف عن تعريف المولارية الذي يعتمد على حجم معين من المحلول.
الوحدة الشائعة للموليالية في الكيمياء هي مول / كغم. يُعبر أحيانًا عن محلول بتركيز 1 مول / كغ على أنه 1 مول. يتشكل مصطلح المولالية بالتشابه مع المولارية وهي التركيز المولي لمحلول ما.
يمكن اختبار مولالية المحلول بإضافة بعض المذيب. بشكل أكثر بساطة ، مولالية (م) من المحلول هي مولات المذاب مقسومة على كيلوغرامات المذيب. المولالية أو المولالية هي تركيز المحلول الذي يحدد عدد مولات المذاب في 1 كجم أو 1000 جرام من المذيب.
الفرق بين المولارية والمولارية هو أنه إذا كانت المولارية هي المولالية أو أن التركيز المولي (م) يعبر عن عدد الشامات المذاب في 1000 جرام من المذيب بينما المولارية هي بيان لعدد مولات المذاب في كل لتر واحد حل. يتم تمثيل المولارية بالرمز M والوحدات هي مولات / لتر.
صيغة مولالي
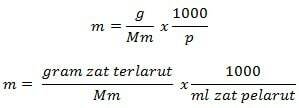
معلومة
م = مولالي (مول / كغ)
ز = غرام من المذاب (غ)
مم = الكتلة المولية للمادة (جم / مول)
P = كتلة المذيب (جم)
علاقة مولالية مع نسبة الكتلة
نسبة الكتلة هي وحدة تركيز شائعة الاستخدام في المحاليل الكيميائية. من الأمثلة على الحلول التي يمكن أن نجدها كل يوم محلول كحول 75٪ و 24٪ محلول حمض أسيتيك. نسبة الكتلة هي عدد جرامات المذاب في 100 جرام من كتلة المحلول. المعادلة التي توضح حساب نسبة الكتلة هي كما يلي:

علاقة المولودة بالمولارية
تعبر المولارية عن عدد مولات المذاب في لتر واحد من المحلول. يمكن تحويل المولارية إلى مولارية عن طريق تحويل حجم المحلول إلى كتلة المحلول. يتطلب تحويل الحجم إلى كتلة بيانات عن كثافة المحلول (p) ، والتي يمكن صياغتها على النحو التالي:

الكسر المولي
جزء الخلد هو مقياس لتركيز المحلول الذي يعبر عن نسبة عدد المولات في جزء من المادة إلى العدد الإجمالي للمولات الموجودة في مكونات المحلول. ينقسم جزء الخلد إلى جزأين:
جزء الخلد المذاب (Xt)
صيغة الكسر الجزيئي للمذاب (Xt) ، وهي:

معلومة:
Xt = جزء الخلد من المذاب
Nt = عدد مولات المذاب
Np = عدد مولات المذيب
جزء الخلد المذيب (Xp)
صيغة الجزء الجزيئي للمذيب (Xp) ، وهي:

معلومة
Xp = جزء الخلد من المذيب
Nt = عدد مولات المذاب
Np = عدد مولات المذيب
مجموع الكسور الجزيئية للمذاب والمذيب هو 1
Xt + Xp = 1
أمثلة على مشاكل المولالي وحلولها
المشكلة 1
ما هي مولالية محلول يحتوي على 4 جم من هيدروكسيد الصوديوم (Ar Na = 23 جم / مول ، Ar O = 16 جم / مول ، و Ar H = 1 جم / مول) مذاب في 250 جم من الماء؟
انتهاء:
معروف:
كتلة هيدروكسيد الصوديوم = 4 غرام
أرنا = 23 غرام / مول
ArO = 16 جم / مول
ArH = 1 غرام / مول
كتلة الماء = 250 جم = 0.25 كجم
سئل: م =؟
إجابة:
السيد. هيدروكسيد الصوديوم = 40 جم / مول
عدد مولات هيدروكسيد الصوديوم = الكتلة / السيد
عدد مولات هيدروكسيد الصوديوم = 4 غرام / (40 غرام / مول)
عدد مولات هيدروكسيد الصوديوم = 0.1 مول
م = عدد المولات / ع
م = 0.1 مول / 0.25 كجم
م = 0.4 م
المشكلة 2
ما هو مولالي 37٪ (وزن / وزن) محلول حمض الهيدروكلوريك؟ (Ar H = 1 جم / مول ، Ar H = 35.5 جم / مول)
انتهاء:
معروف:
كتلة حمض الهيدروكلوريك = 37٪
ArH = 1 جم / مول
ArCl = 35.5 جم / مول
سئل: م =؟
إجابة:
السيد. حمض الهيدروكلوريك = 36.5 غرام / مول
لنفترض أن كتلة المحلول 100 جرام ، فإن كتلة حمض الهيدروكلوريك هي:
كتلة حمض الهيدروكلوريك = 37٪ × 100 غرام
كتلة حمض الهيدروكلوريك = 37 غرام
كتلة المذيب = كتلة المحلول - كتلة حمض الهيدروكلوريك
كتلة المذيب = 100 غرام - 37 غرام
كتلة المذيب = 63 جم = 0.063 كجم
عدد مولات حمض الهيدروكلوريك = الكتلة / السيد
عدد مولات حمض الهيدروكلوريك = 37 غرام / (36.5 غرام / مول)
عدد مولات حمض الهيدروكلوريك = 1.01 مول
م = عدد المولات / كتلة المذيب
م = 1.01 مول /0.063 كجم
م = 16.03 م
مشكلة 3
حدد مولالية المحلول المحضر بإذابة 12 جرامًا من اليوريا CO (NH2) 2 في 250 جرامًا من الماء.
انتهاء:
معروف:
كتلة اليوريا = 12 غرام
مستر يوريا = 60 جم / مول
كتلة المذيب = 250 جم = 0.25 كجم
سئل: م =؟
إعلان
إجابة:
عدد مولات اليوريا = الكتلة / السيد
عدد مولات اليوريا = 12 غرام / (60 جم / مول)
عدد مولات اليوريا = 0.2 مول
م = عدد المولات / كتلة المذيب
م = 0.2 مول / 0.25 كجم
م = 0.8 م
المشكلة 4
ما هي مولالي المحلول الكحولي الذي يحتوي على 23٪ كتلة من الإيثانول (السيد = 46)؟
إجابة:
معروف:
كتلة الإيثانول = 23٪
السيد الإيثانول = 46 جم / مول
سئل: م =؟
انتهاء:
على سبيل المثال كتلة محلول الكحول 100 جرام ، كتلة الإيثانول هي:
كتلة الإيثانول = 23٪ × 100 غرام
كتلة الإيثانول = 23 غرام
كتلة المذيب = كتلة المحلول - كتلة الإيثانول
كتلة المذيب = 100 جم - 23 جم
كتلة المذيب = 77 غرام = 0.077 كجم
عدد مولات الإيثانول = الكتلة / السيد
عدد مولات الإيثانول = 23 غرام / (46 جم / مول)
عدد مولات الإيثانول = 0.5 مول
م = عدد المولات / كتلة المذيب
م = 0.5 مول /0.077 كجم
م = 6.49 م
المشكلة 5
احسب تركيز الجلوكوز (٪ بالكتلة) في محلول جلوكوز 2 مول.
انتهاء:
معروف:
م = 2 مول = 2 مول / كجم = 0.002 مول / غرام
مستر جلوكوز = 180 جم / مول
طلبت: كتلة الجلوكوز (٪) =؟
إجابة:
مولات الجلوكوز = الكتلة / السيد
مولات الجلوكوز = كتلة الجلوكوز / (180 جم / مول)
مولات الجلوكوز = كتلة الجلوكوز × 0.005 مول / غرام
استبدل مولات الجلوكوز بالمعادلة التالية:
م = مولات الجلوكوز / كتلة المذيب
0.002 = كتلة الجلوكوز × 0.005 / كتلة المذيب
o، oo2 / o، oo5 = كتلة الجلوكوز / كتلة المذيب
2/5 = كتلة الجلوكوز / كتلة المذيب
لذا فإن نسبة كتلة الجلوكوز: كتلة المذيب = 2: 5 ، بينما نسبة كتلة الجلوكوز: كتلة المحلول = 2: 7.
لذا،
النسبة المئوية لكتلة الجلوكوز = (كتلة الجلوكوز / كتلة المحلول) × 100٪
٪ من كتلة الجلوكوز = (2/7) × 100٪
٪ كتلة الجلوكوز = 28.57٪
المشكلة 6
ما هي مولالية محلول يحتوي على 8 جم من هيدروكسيد الصوديوم (Ar Na = 23 جم / مول ، Ar O = 16 جم / مول ، و Ar H = 1 جم / مول) مذاب في 250 جم من الماء؟
مناقشة
معروف:
كتلة هيدروكسيد الصوديوم = 8 غرام
أرنا = 23 غرام / مول
ArO = 16 جم / مول
ArH = 1 غرام / مول
كتلة الماء = 250 جم = 0.25 كجم
مطلوب: مولالي (م) ...؟
إجابة:
السيد. هيدروكسيد الصوديوم = 40 جم / مول
عدد مولات NaOH = الكتلة / السيد
عدد مولات هيدروكسيد الصوديوم = 8 غرام / (40 غرام / مول)
عدد مولات هيدروكسيد الصوديوم = 0.2 مول
م = عدد المولات / ع
م = 0.2 مول / 0.25 كجم
م = 0.8 م
المشكلة 6
حدد مولالية المحلول المحضر بإذابة 15 جرامًا من اليوريا CO (NH2) 2 في 250 جرامًا من الماء.
مناقشة
معروف:
كتلة اليوريا = 15 غرام
مستر يوريا = 60 جم / مول
كتلة المذيب = 250 جم = 0.25 كجم
مطلوب: مولالي (م)…. ?
إجابة:
عدد مولات اليوريا = الكتلة / السيد
مجموع مولات اليوريا = 15 جم / 60 جم / مول
عدد مولات اليوريا = 0.25 مول
م = عدد المولات / كتلة المذيب
م = 0.25 مول / 0.25 كجم
م = 1 م
المشكلة 7
ما هو مولالي 37٪ (وزن / وزن) محلول حمض الهيدروكلوريك؟ (Ar H = 1 جم / مول ، Ar H = 35.5 جم / مول).
مناقشة
معروف:
كتلة حمض الهيدروكلوريك = 37٪
ArH = 1 جم / مول
ArCl = 35.5 جم / مول
مطلوب: مولالي (م) ...؟
إجابة:
السيد. حمض الهيدروكلوريك = 36.5 غرام / مول
لنفترض أن كتلة المحلول 100 جرام ، فإن كتلة حمض الهيدروكلوريك هي:
كتلة حمض الهيدروكلوريك = 37٪ × 100 غرام
كتلة حمض الهيدروكلوريك = 37 غرام
كتلة المذيب = كتلة المحلول - كتلة حمض الهيدروكلوريك
كتلة المذيب = 100 غرام - 37 غرام
كتلة المذيب = 63 جم = 0.063 كجم
عدد مولات حمض الهيدروكلوريك = الكتلة / السيد
عدد مولات حمض الهيدروكلوريك = 37 غرام / (36.5 غرام / مول)
عدد مولات حمض الهيدروكلوريك = 1.01 مول
م = عدد المولات / كتلة المذيب
م = 1.01 مول /0.063 كجم
م = 16.03 م

المشكلة 8
حدد كمية (جرامات) من هيدروكسيد الصوديوم التي يجب إذابتها في لتر واحد من الماء (الماء = 1.00 جم / مل) للحصول على 0.25 م هيدروكسيد الصوديوم.
مناقشة
معروف:
1 لتر من الماء = 1000 مل = 1000 جم (حيث أن من الماء = 1.00 جم / مل)
mNaOH = 0.25 م
السيد NaOh = 40
سئل: غرام ...؟
إجابة:
mNaOH = غرام / السيد × 1،000 / ف
0.25 = غرام / 40 × 1،000 / 1،000
0.25 = جم / 40
ج = 0.25 × 40
ز = 10 جرام
لذا ، فإن كمية هيدروكسيد الصوديوم المطلوبة هي 10 جرام.
المشكلة 9
حدد عدد مل من الماء المطلوب لإذابة 4.9 جرام من H2SO4 الذي يكون تركيزه 0.25 M (Ar H = 1 ؛ S = 32 ؛ س = 16)!
مناقشة
معروف:
mH2SO4 = 0.25
السيد H2SO4 = 98
غرام = 4.9 جرام
سئل: ص ؟؟؟
إجابة:
م = غرام / السيد × 1،000 / ف
0.25 = 4.9 / 98 × 1،000 / ع
ع = 20 جرام (20 مل)
إذن ، حجم الماء 20 مل.
المشكلة 10
ما كتلة الماء المطلوبة لتحضير محلول 1.2 م باستخدام 0.6 مول كلوريد الصوديوم؟
مناقشة
مولالية (م) = 1.2 مم =
نص
1,2 =
0,6ص
ف =
0,61,2
= 0.5 كجم
لذا فإن كتلة الماء (كتلة المذيب) المطلوبة هي 0.5 كجم
المشكلة 11
افترض أن هناك 2 مول من المذاب مذاب في 1 لتر من المذيب ، ما هي المولالية؟
مناقشة
مولات مذابة (ن) = 2 مولم =
نص
م =
21
= 2 م
احسب مولالي 25 جرامًا من KBr (Mr = 119) مذابًا في 750 مل من الماء النقي.
مناقشة
المذاب = 25 جرام
السيد = 119
المذيب (P) = 750 مل = 750 جرام (لأن ρ من الماء = 1.00 جم / مل) = 0.75 كجم ن =
مادة ذائبةالسيد
ن =
25119
= 0.21 مول
م =
نص
م =
0,210,75
= 0.28 م
وبالتالي فإن المراجعة من حول Knowledge.co.id عن مثال على مشكلة مولية , نأمل أن تضيف إلى بصيرتك ومعرفتك. شكرا لزيارتك ولا تنسى قراءة مقالات أخرى.
قائمة المحتويات
توصية:
- السليلوز هو: التعريف والنوع والبنية والخصائص و ... السليلوز هو: التعريف ، النوع ، الهيكل ، الخصائص والوظائف - السليلوز مركب شبيه بالألياف ، ويوجد في جدران الخلايا الواقية للنباتات. لفهم أفضل ، سنناقش بالطبع ...
- √ تعريف التمدد في الطول والصيغة والمساحة وحجم المادة ... تعريف التمدد الطويل والصيغ ومساحة وحجم المواد الصلبة - في هذه المناقشة سنشرح حول التوسع الطويل. والذي يتضمن فكرة التوسع الطويل ، صيغ التوسع الطويل ، المساحة ، حجم المادة ...
- المقاييس: التعريف ، تحويل وحدة الطول ، كيفية ... قياس السلم: التعريف ، وتحويل وحدات الطول ، وكيفية الاستخدام ، وأمثلة على الأسئلة - ما هو موجود ماذا تقصد بحجم السلم وكيفية استخدامه ؟، هذه المرة حول Knowledge.co.id will ناقشها ...
- الروابط التساهمية: التعريف ، الخصائص ، الأنواع ، الصيغ ... الروابط التساهمية: التعريف ، الخصائص ، الأنواع ، الصيغ الكيميائية وخصائص المركبات - ما هي الرابطة التساهمية؟ في هذه المناسبة ، سوف يناقش Seputarknowledge.co.id ذلك وبالطبع حول أشياء أخرى أيضًا غطتها. يترك…
- الخطاب البيئي: التعريف والغرض والخصائص و ... الخطاب البيئي: التعريف والغرض والخصائص والأمثلة - كيف يتم بناء نص الخطاب البيئي؟ ما هو الخير والصحيح ؟، في هذه المناسبة ، سوف يناقش Seputarknowledge.co.id ذلك وبالطبع الأمور أيّ…
- الصيغ المخروطية وخصائصها وخصائصها وعناصرها وأمثلة على المشكلات مشكلة الصيغ المخروطية والخصائص والخصائص والعناصر والأمثلة - كيفية حساب مساحة الشكل وحجمه مساحة مخروطية ؟، في هذه المناسبة ، سوف يناقش Seputarknowledge.co.id ذلك وبالطبع عن أشياء أخرى أيّ…
- صيغة اللزوجة: تعريف اللزوجة والمعامل و ... صيغة اللزوجة: تعريف اللزوجة والمعامل والعوامل المؤثرة - كيف هي صيغة اللزوجة هل هو؟ اللزوجة هي قياس مقاومة السائل الذي يتغير إما عن طريق الإجهاد أو عن طريق ضغط. بهذه المناسبة ، Seputarknowledge.co.id ...
- وحدة الوزن: التعريف وسلم التحويل وأمثلة ... وحدة الوزن: التعريف وسلم التحويل ومثال المشكلة - ما هي وحدة الوزن ؟، في هذه المناسبة حول Knowledge.co.id سيناقشها ، بما في ذلك الفهم وبالطبع أشياء أخرى أيضًا غطتها. يترك…
- لحظة القصور الذاتي: التعريف ، العوامل ، معادلات النماذج ... لحظة القصور الذاتي: التعريف والعوامل والمعادلات في أشكال الكائنات وأمثلة المشكلات - ما هو المقصود مع لحظة القصور الذاتي ؟، في هذه المناسبة ، سيناقش Se بخصوص Knowledge.co.id ذلك وبالطبع حول موضوع…
- التغيير المنتظم للحركة الدائرية: التعريف ، الحجم ... التغيير المنتظم للحركة الدائرية: التعريف والكمية المادية والصيغ وأمثلة على المشكلات - ما هي الحركة التغييرات الدورية والأمثلة بشكل منتظم؟ في هذه المناسبة ، سوف يناقش Seputarknowledge.co.id ذلك و بالطبع عن ...
- تكامل غير محدد: التعريف والصيغ والخصائص والأمثلة ... تكامل غير محدد: التعريف والصيغ والخصائص وأمثلة على المشاكل - ما المقصود بالتكامل غير المحدد طبعا وكيف تحسب العمليات الحسابية؟ سوف…
- تعريف طرق التعلم: الخصائص والغرض والأنواع و ... تعريف طرق التعلم: الخصائص والغرض والأنواع والمناقشة - المقصود بالطريقة التعلم؟ ، في هذه المناسبة ، سوف يناقش Seputarknowledge.co.id ذلك وبالطبع عن أشياء أخرى أيضًا…
- التوازن الكيميائي: التعريف ، القوانين ، الصيغ ، أمثلة على المشكلات التوازن الكيميائي: التعريف ، القوانين ، الصيغ ، أمثلة على المشكلات - في هذه المناقشة سنشرح حول التوازن الكيميائي وقانون الصيغة ومجهز بأمثلة للتوازن الكيميائي مع ...
- الحلول الحمضية القاعدية: التعريف ، نظرية القاعدة الحمضية ، الخصائص و ... الحلول الحمضية القاعدية: التعريف ، نظرية القاعدة الحمضية ، الخصائص والأنواع - الحلول الحمضية والقاعدية هي مجموعتان من المركبات الكيميائية التي توجد على نطاق واسع وتستخدم في الحياة اليومية.
- بناء مساحة - التعريف والصيغ ومختلف ... بناء الفضاء - التعريف والصيغ وأنواعها المختلفة - في هذه المناسبة ، نود مراجعة المواد الرياضية حول الأشكال الهندسية ، من حيث الفهم وغيرها. على الفور ، دعنا نناقش ...
- √ مؤشر القاعدة الحمضية: التعريف والأنواع والأمثلة مؤشرات القاعدة الحمضية: التعريف والأنواع والأمثلة - في هذه المناسبة ، ستناقش شركة حول المعرفة مؤشرات القاعدة الحمضية. والذي في هذه المناقشة يشرح معنى المؤشر الحمضي ...
- قانون بويل: التعريف والصيغ والتطبيقات والأمثلة ... قانون بويل: التعريف والصيغ والتطبيقات وأمثلة على المشكلات - في هذه المناقشة سنشرح قانون بويل. والذي يتضمن معنى قانون بويل ، وصيغة قانون بويل ، وتطبيق ...
- القصص القصيرة التحفيزية: التعريف ، كتابة النصائح والأمثلة القصص القصيرة التحفيزية: التعريف ، نصائح وأمثلة للكتابة - ما هي القصة القصيرة التحفيزية ؟، على في هذه المناسبة ، سوف يناقش موقع Seputarknowledge.co.id ما إذا كانت القصة القصيرة للصداقة ومسائل أخرى حوله. دعنا نرى…
- تعريف الضغط: أنواع الضغط والصيغ وأمثلة على المشاكل تعريف الضغط: أنواع الضغط والصيغ وأمثلة على المشكلات - ما هو الضغط؟ في هذه المناسبة ، حول Knowledge.co.id ، سنناقش ماهية الضغط وما هي العناصر الأخرى غطتها. دعنا نرى…
- السوائل الديناميكية: الأنواع ، الميزات ، معادلة برنولي ، النظريات ... السوائل الديناميكية: الأنواع ، الخصائص ، معادلة برنولي ، نظرية توريتشيلي ، الصيغ وأمثلة على المشاكل - ما هي السوائل الديناميكية وأنواعها؟ عن…
- كثافة الماء: التعريف والصيغ والأمثلة كثافة الماء: التعريف والصيغ والأمثلة - ما هي كثافة الماء؟ لنرى معا ...
- تعريف الكمية والوحدة والقياس والأمثلة ... تعريف الكمية والوحدة والقياس والأمثلة (كاملة) - في مفاهيم الفيزياء الأساسية ، من المؤكد أننا تعرفنا على شيء يتعلق بالحياة اليومية. مثل قياس الطول ، وزن الكتلة ، قياس العرض ، ...
- أمثلة على العمل العلمي: وظائف وقواعد اللغة أمثلة من الأوراق العلمية: وظائف اللغة وقواعدها - ما هي أمثلة الأشكال الجيدة والصحيحة لكتابة الأوراق العلمية؟ سابقًا ، ناقش Seputar the Knowledge.co.id العمل العلمي: التعريف ، الخصائص ، الفوائد ، ...
- أمثلة على الأشكال المسطحة: أنواع وخصائص وصيغ الأشكال المسطحة أمثلة على الأشكال المسطحة: أنواع وخصائص وصيغ الأشكال المسطحة - ما هي أمثلة الأشكال المسطحة؟
- عينة من أسئلة التربية البدنية للفصل 11 (XI) SMA / MA / SMK الفصل 1 و 2 أمثلة على أسئلة التربية البدنية للفصل 11 (XI) لـ SMA / MA / SMK الفصل الدراسي 1 و 2 (2019 و 2020) - في هذه المناسبة ، سوف يناقش Seputarknowledge.co.id أمثلة على أسئلة التربية البدنية للفصل 11 الاختيار من متعدد والمقال ...
- الهطول: 12 تعريفات حسب الخبراء ، أنواع ، ... هطول الأمطار هو: 12 تعريفًا وفقًا لأنواع وعوامل الخبراء - في هذه المناقشة ، سوف تشرح حول المعرفة حول هطول الأمطار. الامطار حدث مناخي طبيعي ...
- √ تعريف المركبات الكيميائية وخصائصها وأنواعها وتسميتها ... تعريف المركبات الكيميائية ، الخصائص ، الأنواع ، التسمية الكاملة - في هذه المناقشة سنشرح حول المركبات الكيميائية. يغطي تعريف وخصائص وأنواع وتسميات المركبات الكيميائية مع مناقشة ...
- المواد المفردة هي: التعريف والعناصر والمركبات المواد المفردة هي: التعريفات والعناصر والمركبات - ماذا تعني مادة واحدة؟ لنلق نظرة على المناقشة معًا ...
- المستوى المائل: التعريف والصيغ والميزة الميكانيكية و ... المستوى المائل: التعريف والصيغ والمزايا الميكانيكية وأمثلة على المشاكل - ما هو المقصود بالطائرة المائل وكيفية حساب الفيزياء؟ بطبيعة الحال…
- تحويل الوحدة: التعريف ، العامل ، الطول ، الكتلة ، الوقت ، ... تحويل الوحدة: التعريف والعامل والطول والكتلة والوقت والحجم والضغط - ما هو تحويل الوحدة ؟، في هذه المناسبة ، سوف يناقش Seputarknowledge.co.id ذلك ، بما في ذلك العوامل والأنواع وأشياء أخرى بالطبع أيّ…
